题目内容
3.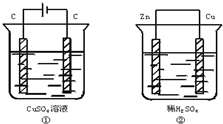 如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )
如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )| A. | 产生气体的体积:①>② | |
| B. | 电极总质量的变化:①增加,②减小 | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | 电极反应式:①装置中的阳极:4OH--4e-→2H2O+O2↑ ②装置中的负极:2H++2e-→H2↑ |
分析 ①有外接电源,所以是电解池,阳极反应为2Cl--2e-=Cl2↑,阴极反应为:Cu2++2e-=Cu,②为原电池,正极反应为2H++2e-=H2↑,负极反应为Zn-2e-=Zn2+,以此解答该题.
解答 解:A、①的阳极反应:2Cl--2e-=Cl2↑,导线中通过0.02mol电子时,产生氯气的体积V=nVm=0.01mol×22.4L/mol=0.0224L,②中的正极反应为:2H++2e-=H2↑,导线中通过0.02mol电子时,产生氢气的体积V=nVm=0.01mol×22.4L/mol=0.0224L,所以产生气体的体积:①=②,故A错误;
B、①中阴极生成铜,②生成氢气,则电极上析出物质的质量变化为:①增加,②减小,故B正确;
C、①相当于电解氯化铜,溶液的pH几乎不变,②相当于锌和硫酸中的氢离子反应,所以氢离子减少,酸性减弱,所以pH增大,故C错误;
D、①中阳极:2Cl--2e-=Cl2↑,②中的正极反应为:2H++2e-=H2↑,故D错误.
故选B.
点评 本题是一道有关原电池和电解池的工作原理的综合题目,要求学生熟悉教材基本知识,具备分析和解决问题的能力.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
14.现有42gFe(NO3)2与Fe(NO3)3的混合物,其中含氮元素7g,则混合物中铁元素的质量为( )
| A. | 14g | B. | 9g | C. | 11g | D. | 7g |
18.下列化学用语完全正确的一组是( )
| A. | 电子式:次氯酸: ;过氧化钠: ;过氧化钠: ;羟基: ;羟基: | |
| B. | KHSO4熔融电离:KHSO4=K++H++SO42-;KHCO3溶解于水:KHCO3=K++H++CO32- | |
| C. | 高聚物化学式:聚异戊二烯: ;PVC: ;PVC: ;PE: ;PE: | |
| D. | 下列分子式代表的有机物均有可能与NaHCO3反应放出CO2:C5H12O2、C2H4O2、C7H8O |
8.下列各组物质属同素异形体的是( )
| A. | 金刚石、石墨和C60 | B. | 16O和18O | ||
| C. | O2和SO3 | D. | H2O和H2O2 |
15.下列物质中属于电解质的是( )
| A. | SO3 | B. | NaCl | C. | O2 | D. | 稀硫酸 |
1.下列液体均处于25℃,有关叙述正确的是( )
| A. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 25℃时,用pH试纸测定出某醋酸溶液的pH=3.50 | |
| D. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在:K+、Na+、AlO2-、SO42- |
2.2002年12月26日,俄罗斯特种部队使用强力麻醉剂芬太奴(Fentanyl)和氟烷(Halothane).下列有关氟烷(CHClBr-CF3)说法正确的是( )
| A. | 该氟烷易溶于水,也易溶于有机溶剂 | |
| B. | 该氟烷扩散到空气中能破坏臭氧层 | |
| C. | 该氟烷密度比水小 | |
| D. | 与该氟烷互为同分异构体的氟烷(不含本身)有三种 |
