题目内容
4.化学与生活密切相关.下列有关说法错误的是( )| A. | SiO2、MgO熔点高,可用于制作耐高温仪器 | |
| B. | 纤维素属于多糖类物质,但不能作人类的营养物质 | |
| C. | 硝酸铵属于氧化剂,严禁用可燃物(如纸袋)包装 | |
| D. | 天然气是可再生清洁能源,可用于工业制盐酸 |
分析 A.耐高温仪器应具有熔点高的性质;
B.纤维素在人体内不能消化;
C.硝酸铵在有可被氧化的物质(还原剂)存在的条件下发生氧化还原反应,有爆炸的危险;
D.天然气属于化石燃料,是不可再生能源.
解答 解:A.SiO2、MgO熔点高,一般条件下不易熔融,所以可以用于制作耐高温仪器,故A正确;
B.人体不含纤维素酶,纤维素在人体内不能消化,不能作人类的营养物质,故B正确;
C.硝酸铵属于氧化剂,应储存于阴凉、通风的库房,远离火种、热源,应与易(可)燃物、还原剂、酸类、活性金属粉末分开存放,故C正确;
D.天然气属于不可再生的清洁能源,故D错误.
故选D.
点评 本题考查了化学知识在生活实际的应用,为高考常见题型,熟悉物质的组成、性质、用途等即可解答,题目有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.将1mol CH4和适量的O2在密闭容器中点燃,充分反应后CH4和O2均无剩余,产物的总质量为72g,且均为气体(101kPa,120℃),下列有关叙述不正确的是( )
| A. | 反应中消耗O2 56 g | |
| B. | 所得产物中各物质的物质的量相等 | |
| C. | 若将产物通过碱石灰,不能被完全吸收 | |
| D. | 若将产物通过浓硫酸,充分吸收后,浓硫酸增重36g |
15.下列生活中常见物质的用途与其还原性有关的是( )
| A. |  碘酒中的碘 | B. |  暖宝宝中的铁粉 | ||
| C. |  抗酸药中的氢氧化铝 | D. |  尿不湿中的聚丙烯酸钠 |
12.下列各组离子在相应的条件下可能大量共存的是( )
| A. | pH=1的溶液中:CO32-、K+、Cl-、Na+ | |
| B. | 由水电离产生的c(OH-)=1×10-13mol•L-1的溶液中:NO3-、Mg2+、Na+、SO42- | |
| C. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- | |
| D. | 含Al3+的溶液中:Na+、HCO3-、Cl-、K+ |
19.CH2=CH2与H2反应的能量与反应进程关系如图所示.下列说法错误的是( )

| A. | 该反应为放热反应 | |
| B. | 催化剂Ⅱ比催化剂Ⅰ活性更好 | |
| C. | 催化剂可改变反应的活化能和焓变 | |
| D. | 正反应的活化能小于逆反应的活化能 |
9.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E,B与F同主族,E与F同周期;D的核电荷数是F的最外层电子数的2倍;B的最高正价与最低负价的代数和为0;常温下单质A与E的状态不同.下列判断正确的是( )
| A. | A、D两种元素形成的化合物中只含有极性键 | |
| B. | A、C、D三种元素形成的化合物一定是共价化合物,其溶液一定呈酸性 | |
| C. | 六种元素中,最高价氧化物对应水化物酸性最强的元素是C | |
| D. | 原子半径由大到小的顺序是F>E>C>D |
5.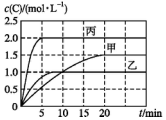 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:
下列说法正确的是( )
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | 1.0 L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
| A. | 10 min内甲容器中反应的平均速率v(A)=0.025 mol•L-1•min-1 | |
| B. | 由图可知:T1<T2,该反应为吸热反应 | |
| C. | x=1,若平衡时保持温度不变,改变容器体积平衡不移动 | |
| D. | T2℃时,丙容器比乙容器反应快的原因是使用了催化剂 |
3.下列有关原电池的叙述正确的是( )
| A. | 原电池是将电能转化为化学能的装置 | |
| B. | 手机所用的锂离子电池属于一次电池 | |
| C. | 可将反应2FeCl3+Cu=2FeCl2+CuCl2设计为原电池 | |
| D. | 铜、锌、稀硫酸原电池工作时,电子通过导线由Cu→Zn |