题目内容
17.有A、B、C、D、E五种短周期元素,其元素特征信息如表:| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
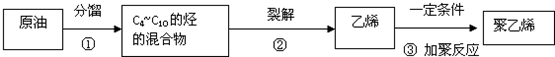
(2)写出A、B、C形成的化合物的电子式
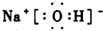 .
.(3)①写出E单质与A、B、C形成的化合物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:2Al+2H2O+2OH-═2AlO2-+3H2↑.
分析 A的单质是密度最小的物质,则AH元素;B的阴离子带两个单位负电荷,单质是空气的主要成分之一,则B为O元素;C的阳离子与B的阴离子有相同的电子层结构,氧离子含有两个电子层,则C处于第三周期的金属元素,且与B可以形成两种离子化合物,则C为Na元素;D的氢氧化物和氧化物都有两性,与C同周期,则D为Al元素;E与C同周期,原子半径在该周期最小,则E处于第三周期,为Cl元素,以此解答该题.
解答 解:A的单质是密度最小的物质,则AH元素;B的阴离子带两个单位负电荷,单质是空气的主要成分之一,则B为O元素;C的阳离子与B的阴离子有相同的电子层结构,氧离子含有两个电子层,则C处于第三周期的金属元素,且与B可以形成两种离子化合物,则C为Na元素;D的氢氧化物和氧化物都有两性,与C同周期,则D为Al元素;E与C同周期,原子半径在该周期最小,则E处于第三周期,为Cl元素,
(1)由分析可知,C为钠、DE为氯元素,故答案为:钠;氯;
(2)A为氢元素、B为氧元素、C为钠元素,A、B、C形成的化合物M为氢氧化钠,电子式为: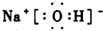 ,
,
故答案为: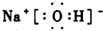 ;
;
(3)①氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的化学方程式为Cl2+2NaOH═NaCl+NaClO+H2O,故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;
②D单质是Al,A、B、C形成的化合物的水溶液是氢氧化钠溶液,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,则反应的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑.
点评 本题考查了位置、结构与性质关系的应用,题目难度中等,推断各元素为解答关键,注意掌握元素周期表结构、元素周期律内容,试题充分考查了学生灵活应用基础知识的能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 2.3g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA | |
| B. | 1molNa2CO3晶体中含CO32-离子数小于NA | |
| C. | 惰性电极电解食盐水,若线路中通过NA电子电量,则阳极产生气体11.2L | |
| D. | 0.1molCaO2(过氧化钙)中含阴离子数是0.2NA |
| A. | 原子数目相等的三种气体,质量最大的是Z | |
| B. | 相同条件下,同质量的二种气体,气体密度最小的是X | |
| C. | 若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1mol | |
| D. | 同温下,体积相同的两容器分别充2 g Y气体和l g Z气体,则其压强比为2:1 |
| A. | T1(OH)3是两性氢氧化物 | B. | 铊与酸反应比铝更剧烈 | ||
| C. | Tl3+的氧化能力比Al3+弱 | D. | 铊是易导电的银白色金属 |
 ,过氧化氢的电子式
,过氧化氢的电子式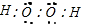 .
.
 ,
,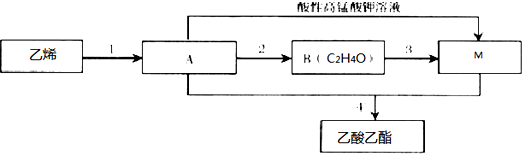
 看如图完成下面的填空,写出电极反应式和总反应式.
看如图完成下面的填空,写出电极反应式和总反应式. J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.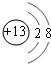 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族. ,R、T的氢化物的稳定强的HCl(填化学式)
,R、T的氢化物的稳定强的HCl(填化学式)