题目内容
6.铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )| A. | T1(OH)3是两性氢氧化物 | B. | 铊与酸反应比铝更剧烈 | ||
| C. | Tl3+的氧化能力比Al3+弱 | D. | 铊是易导电的银白色金属 |
分析 铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,利用同主族元素的性质变化规律来解答.
解答 解:A.同主族从上到下金属性增强,则Tl(OH)3碱性比氢氧化铝强,所以Tl(OH)3是强碱,故A错误;
B.属性Tl>Al,所以铊与酸反应比铝更剧烈,故B正确;
C.金属性Tl>Al,则Tl3+的氧化能力比Al3+弱,故C正确;
D.铝为银白色金属,Tl与Al同主族,则铊是易导电的银白色金属,故D正确.
故选A.
点评 本题考查元素的性质,为高频考点,侧重于学生的分析能力的考查熟悉元素在周期表中的位置及元素周期律是解答本题的关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.有A、B、C、D、E五种短周期元素,其元素特征信息如表:
回答下列问题:(1)写出下列元素的名称:C钠,E氯.
(2)写出A、B、C形成的化合物的电子式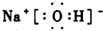 .
.
(3)①写出E单质与A、B、C形成的化合物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:2Al+2H2O+2OH-═2AlO2-+3H2↑.
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(2)写出A、B、C形成的化合物的电子式
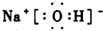 .
.(3)①写出E单质与A、B、C形成的化合物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:2Al+2H2O+2OH-═2AlO2-+3H2↑.
14.下列有关电池的说法中不正确的是( )
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 充电电池可以无限制地反复使用 | |
| C. | 甲醇燃料电池可把化学能转化为电能 | |
| D. | 废旧电池不能乱扔,需回收处理 |
1.用于检验火柴头燃烧可产生SO2的装置正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
11.如表为元素周期表的一部分,其中A、X、Y、W、Z为短周期元素,W元素的核电荷数为X元素的2倍.据此,下列说法中错误的是( )
| X | |||
| Y | Z | W | A |
| T | B |
| A. | X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反 | |
| B. | Y、Z、W、A元素性质均较为活泼,但其中Y、W在自然界中存在游离态的形式,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阳离子交换膜,其阴极反应式为:2H2O+2e-═2OH-+H2↑ | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2W3具有氧化性和还原性 |
18.在某无色溶液中,可能存在Na+、Ca2+、Fe3+、Br-、CO32-、SO42-、Cl-中的几种.某同学进行了下列实验:
①取少量原溶液,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色,将溶液分为2份;
②一份中加入AgNO3溶液,有白色沉淀产生;
③另一份加入BaCl2溶液,有白色沉淀产生.
则该溶液中一定大量存在的离子组是( )
①取少量原溶液,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色,将溶液分为2份;
②一份中加入AgNO3溶液,有白色沉淀产生;
③另一份加入BaCl2溶液,有白色沉淀产生.
则该溶液中一定大量存在的离子组是( )
| A. | Na+、Fe3+、SO42- | B. | CO32-、Cl-、SO42- | C. | Ca2+、Br-、SO42- | D. | Na+、SO42-、CO32- |
1.下列表达正确的是( )
| A. | 氧族元素包括氧、硫、锡、碲、钋 | |
| B. | Na2O2固体中的阳离子和阴离子个数比为1:1 | |
| C. | H、D、T、H+可以用来表示氢元素的四种同位素 | |
| D. | 表示金属元素名称的汉字不一定都含“钅”旁 |
2.下列叙述中,错误的是( )
| A. | 只含非极性键的纯净物一定是单质 | B. | 只含极性键的纯净物一定是化合物 | ||
| C. | 离子化合物中一定有离子键 | D. | 纯净物中一定存在化学键 |