题目内容
17.有二氧化碳与一氧化碳的混合气体共10.8g,其总体积在标况下为6.72L.求:(1)混合气体中二氧化碳与一氧化碳的物质的量各为多少?
(2)混合气体中碳原子与氧原子的物质的量之比为多少.
分析 设出二氧化碳与一氧化碳的物质的量,然后结合二者总质量、标况下体积列式计算,根据计算结果分别计算出混合气体中二氧化碳与一氧化碳的物质的量、碳原子与氧原子的物质的量之比.
解答 解:(1)设混合气体中CO2、CO的物质的量分别为x、y,
则:$\left\{\begin{array}{l}{44x+28y=10.8}\\{x+y=\frac{6.72}{22.4}=0.3}\end{array}\right.$,
解得:$\left\{\begin{array}{l}{x=0.15mol}\\{y=0.15mol}\end{array}\right.$
答:混合气体中含有0.15 molCO、0.15 mol CO2;
(2)混合气体中碳原子与氧原子的物质的量之比=(0.15mol+0.15mol):(0.15mol×2+0.15mol)=2:3,
答:混合气体中碳原子与氧原子的物质的量之比为2:3.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积之间的关系为解答关键,试题培养了学生的化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.在下列溶液中分别放入铁棒,过一会儿把铁棒取出,(1)能使铁棒质量增加的溶液是____;(2)溶液质量增加的是______.( )
| A. | 稀硫酸 | B. | 食盐水 | C. | 硫酸铜溶液 | D. | 乙醇水溶液 |
12.下列说法正确的是( )
| A. | 用过滤的方法可以除去食盐水中的泥沙 | |
| B. | 酒精灯加热烧瓶时不用垫石棉网 | |
| C. | 氯化氢气体能使干燥的蓝色石蕊试纸变红 | |
| D. | 盛放氢氧化钠溶液的玻璃瓶,可以使用橡胶塞或玻璃塞 |
2.如图所示甲、乙是实验室试剂标签上的部分内容,下列说法正确的是( )

| A. | 该氨水的物质的量浓度约为6.3mol•L-1 | |
| B. | 各取5ml与等质量的水混合后,c(H2SO4)<9.2 mol•L-1,c(NH3)>6.45 mol•L-1 | |
| C. | 常温下铁不能与该硫酸反应 | |
| D. | 各取10ml于两烧杯中,再分别加入一定量的水即可得到较稀的硫酸溶液和氨水 |
6.下列有关物质性质的应用正确的是( )
| A. | 液氨气化时要吸收大量的热,可用作制冷剂 | |
| B. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| C. | SO2具有氧化性,可用于漂白纸浆 | |
| D. | 氯化铝是一种电解质,可用于电解法制铝 |
7.下列物质一定表示一种纯净物的是( )
| A. | C3H6 | B. | C2H4 | C. | [-CH2-CH2-]n | D. | C4H10 |

 ;
;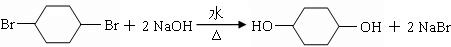 .
.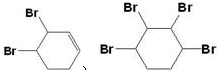 .
.