题目内容
6.下列有关物质性质的应用正确的是( )| A. | 液氨气化时要吸收大量的热,可用作制冷剂 | |
| B. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| C. | SO2具有氧化性,可用于漂白纸浆 | |
| D. | 氯化铝是一种电解质,可用于电解法制铝 |
分析 A.液氨气化时要吸收大量的热,具有制冷作用;
B.二氧化硅与氢氟酸反应生成四氟化硅和水;
C.依据二氧化硫的漂白性解答;
D.熔融氯化铝不导电.
解答 解:A.液氨气化时要吸收大量的热,具有制冷作用,常用作制冷剂,故A正确;
B.二氧化硅与氢氟酸反应生成四氟化硅和水,所以氢氟酸不能用石英器皿盛放,故B错误;
C.二氧化硫可用于漂白纸浆是因为其具有漂白性,与其氧化性无关,故C错误;
D.熔融氯化铝不导电,不能用电解熔融氯化铝的方法制取铝,通常用电解熔融氧化铝的方法制备铝,故D错误;
故选:A.
点评 本题考查了元素化合物知识,熟悉氨气、HF、二氧化硫、氯化铝的性质是解题关键,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
14.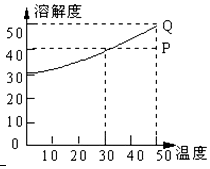 有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )
有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )
 有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )
有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )| A. | 50℃时,若该盐溶液含A克溶质,保持温度不变,加入A/4 g溶质,溶液必变成饱和溶液 | |
| B. | 50℃时,140g P点溶液最少需蒸发掉20g水才能形成饱和溶液 | |
| C. | 该溶液冷却至0℃时,析出溶质10 g | |
| D. | 在保持溶质及溶剂质量不变的情况下,使P点溶液达到饱和需降温20℃ |
11.在温度相同时,100mL0.01mol/L的CH3OOH溶液与10mL0.1mol/LCH3COOH溶液相比较,下列叙述中前者大于后者的是( )
| A. | CH3OOH的物质的量 | |
| B. | 溶液中的n(H+) | |
| C. | 用同浓度的NaOH溶液恰好完全反砬,消耗NaOH溶液的体积 | |
| D. | 溶液的导电能力 |
15.对某难溶电解质AnBm的饱和溶液中,下列说法正确的是( )
| A. | 加水,它的溶度积减小、溶解度增大 | |
| B. | 升高温度,它的溶解度和溶度积都增大 | |
| C. | 饱和溶液中c(Am+)=c(Bn-) | |
| D. | 加水,它的溶度积、溶解度均不变 |
16.下列离子方程式书写正确的是( )
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向Ba(OH)2溶液中加入H2SO4溶液:Ba2++SO42-═BaSO4↓ | |
| C. | 向Na2CO3溶液中加入少量稀H2SO4溶液:CO32-+2H+═CO2↑+H2O | |
| D. | 过量的铁与稀HNO3反应:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |