题目内容
12.下列说法正确的是( )| A. | 用过滤的方法可以除去食盐水中的泥沙 | |
| B. | 酒精灯加热烧瓶时不用垫石棉网 | |
| C. | 氯化氢气体能使干燥的蓝色石蕊试纸变红 | |
| D. | 盛放氢氧化钠溶液的玻璃瓶,可以使用橡胶塞或玻璃塞 |
分析 A.泥沙不溶于水;
B.烧瓶不能直接加热;
C.干燥的氯化氢不能电离出氢离子;
D.不能用玻璃塞.
解答 解:A.泥沙不溶于水,可用过滤的方法分离,故A正确;
B.烧瓶不能直接加热,应垫石棉网,故B错误;
C.干燥的氯化氢不能电离出氢离子,溶液呈酸性,可使湿润的蓝色石蕊试纸变红,故C错误;
D.氢氧化钠和玻璃的中的二氧化硅反应,导致玻璃塞打不开,不能用玻璃塞,故D错误.
故选A.
点评 本题综合考查物质的分离、提纯、仪器的使用和药品的保存,为高考常见题型,侧重考查学生的分析能力和实验能力,注意把握实验的合理性和可行性的评价,难度不大.

练习册系列答案
相关题目
7.下列叙述中,正确的是( )
| A. | C、N、O元素的单质与氢气化合越来越难 | |
| B. | Li、Na、K的氧化物的水化物的碱性依次减弱 | |
| C. | Na、Mg、Al的简单离子的氧化性以依次增强 | |
| D. | P、S、Cl元素的最高正价依次升高,其对应的气态氢化物的稳定性依次减弱 |
3.下列指定反应的离子方程式正确的是( )
| A. | 将铜插入浓硝酸中:Cu+4H++2NO3?═Cu2++2NO2↑+2H2O | |
| B. | 向FeBr2溶液中通入过量氯气:2Fe2++Cl2═2Fe3++2Cl? | |
| C. | 向Al2O3中加入氨水:Al2O3+2OH?═2AlO2?+H2O | |
| D. | 碳和浓硫酸加热:C+2H++SO42?═H2O+SO2↑+CO2↑ |
20.Al、Fe、Cu都是重要的金属元素,下列说法正确的是( )
| A. | 三者对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质放置在空气中均只生成氧化物 | |
| C. | 电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al | |
| D. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
7.下面关于电解质的叙述中错误的是( )
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | 电解质在水中一定能导电,在水中导电的化合物一定是电解质 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
2.有关化合物的Ksp 如表所示(25℃时):
用废电池的锌皮制备ZnSO4•7H2O 的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀H2SO4和H2O2 溶解,铁变为Fe3+,加碱调节至pH 为3.7 时,Fe3+沉淀完全;继续加碱至pH 约为6时,锌开始沉淀(假定Zn2+的浓度为0.1mol•L-1).若上述过程不加H2O2,则Zn2+和Fe2+分离不开,其原因是Zn(OH)2、Fe(OH)2的Ksp相近.
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp | 1×10-17 | 8×10-16 | 4×10-38 |
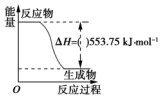 (1)运动会中的火炬一般采用丙烷(C3H8)为燃料.丙烷热值较高,污染较小,是一种优良的燃料.试回答下列问题:
(1)运动会中的火炬一般采用丙烷(C3H8)为燃料.丙烷热值较高,污染较小,是一种优良的燃料.试回答下列问题: