题目内容
8.SiCl4的分子结构与CCl4相似,对其进行下列推测,不正确的是( )| A. | SiCl4晶体是分子晶体 | |
| B. | 常温常压下SiCl4是气体 | |
| C. | SiCl4的分子 是由极性键形成的非极性分子 | |
| D. | SiCl4的熔点高于CCl4 |
分析 SiCl4的分子结构与CCl4类似,与CCl4根据的结构和性质分析,CCl4属于分子晶体,常温为液体,含有共价键,分子晶体的相对分子质量越大,沸点越高,据此分析.
解答 解:SiCl4的分子结构与CCl4类似,与CCl4根据的结构和性质分析,CCl4属于分子晶体,常温为液体,含有共价键,分子晶体的相对分子质量越大,熔点越高,
A、SiCl4与CCl4结构相似,则常温常压下SiCl4是分子晶体,故A正确;
B、SiCl4与CCl4结构相似,常温常压下CCl4是液体,依据结构相似的分子晶体,其熔沸点取决于相对分子质量的大小,相对分子质量越大,熔沸点越高,Si的相对原子质量为28,大于C的为12,故SiCl4是液体不是气体,故B错误;
C、SiCl4中Si与Cl形成共价键,则SiCl4是由极性共价键形成的非极性分子,故C正确;
D、分子晶体的相对分子质量越大,熔点越高,则SiCl4熔点高于CCl4,故D正确;
故选B.
点评 本题考查了物质的结构和性质,采用类比法分析,题目难度不大,注意把握CCl4的结构和性质.

练习册系列答案
相关题目
13.下列仪器名称为“圆底烧瓶”的是( )
| A. |  | B. |  | C. |  | D. |  |
14.下列化学方程式或离子方程式正确的是( )
| A. | 苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | 甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$HCOO-+NH4++2Ag↓+3NH3+H2O | |
| C. | 1一氯丙烷中加入氢氧化钠溶液并加热:CH3CH2CH2Cl+NaOH $→_{△}^{水}$CH3CH=CH2↑+NaCl+H2O | |
| D. | 向小苏打溶液中加入醋酸:HCO3-+CH3COOH═CO2↑+H2O+CH3COO- |
3.往50mL FeBr2溶液中缓慢通入1.12L(标况)Cl2溶液中还有$\frac{2}{3}$的Br-未被氧化,则原FeBr2溶液的物质的量的浓度( )
| A. | 3mol/l | B. | 2.4mol/l | C. | 1.2mol/l | D. | 1mol/l |
13.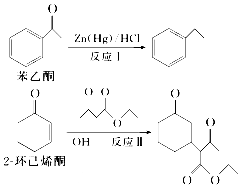 反应Ⅰ和反应Ⅱ都是有机合成中的重要反应:下列有关说法正确的是( )
反应Ⅰ和反应Ⅱ都是有机合成中的重要反应:下列有关说法正确的是( )
 反应Ⅰ和反应Ⅱ都是有机合成中的重要反应:下列有关说法正确的是( )
反应Ⅰ和反应Ⅱ都是有机合成中的重要反应:下列有关说法正确的是( )| A. | 苯乙酮的一氯代物有6种同分异构体 | |
| B. | 苯乙酮经反应Ⅰ所得产物的所有原子不可能在同一平面内 | |
| C. | 反应Ⅱ为取代反应 | |
| D. | 反应Ⅱ可以在强碱性条件下进行 |
20.在无色透明的强酸性溶液中,能大量共存的( )
| A. | Na+、NO3-、Al3+、Cl- | B. | Na+、CO32+、K+、NO3- | ||
| C. | Cu2+、K+、SO42-、Cl- | D. | Ba2+、K+、Cl-、HS- |
17. 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图.下列有关叙述不正确的是( )
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图.下列有关叙述不正确的是( )
 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图.下列有关叙述不正确的是( )
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图.下列有关叙述不正确的是( )| A. | H+从负极区通过交换膜移向正极区 | |
| B. | 电池总反应为2CH3OH+3O2═2CO2+4H2O | |
| C. | 负极的电极反应式为:CH3OH+H2O-6e-=CO2↑+6H + | |
| D. | 图中b、c分别是O2、甲醇 |
18.下列变化中需加入氧化剂才能实现的是( )
| A. | Na2S→H2S | B. | MnO4-→Mn2+ | C. | I-→I2 | D. | ClO-→Cl2 |