题目内容
3.往50mL FeBr2溶液中缓慢通入1.12L(标况)Cl2溶液中还有$\frac{2}{3}$的Br-未被氧化,则原FeBr2溶液的物质的量的浓度( )| A. | 3mol/l | B. | 2.4mol/l | C. | 1.2mol/l | D. | 1mol/l |
分析 n(Cl2)=$\frac{1.12L}{22.4L/mol}$=0.05mol,还原性Fe2+>Br-,所以氯气先氧化Fe2+后氧化Br-,氯气和溴化亚铁充分反应后,有$\frac{2}{3}$的Br-被氧化成Br2,说明亚铁离子完全被氧化,根据转移电子相等进行计算.
解答 解:n(Cl2)=$\frac{1.12L}{22.4L/mol}$=0.05mol,还原性Fe2+>Br-,所以氯气先氧化Fe2+后氧化Br-,氯气和溴化亚铁充分反应后,有$\frac{2}{3}$的Br-被氧化成Br2,说明亚铁离子完全被氧化,
设(FeBr2)=xmol,则溶液中n(Fe2+)=xmol,n(Br-)=2n(FeBr2)=2xmol,根据转移电子相等得n(Cl2)×2=n(Fe2+)×1+$\frac{2}{3}$n(Br-)×1,
即0.05mol×2=xmol×1+$\frac{2}{3}$×2xmol×1,
x=0.06,
c(FeBr2)=$\frac{0.06mol}{0.05L}$=1.mol/L,
故选C.
点评 本题考查氧化还原反应的计算,明确离子还原性先后顺序是解本题关键,结合转移电子守恒进行计算,侧重考查分析问题、计算能力,题目难度不大.

练习册系列答案
相关题目
8.下列物质属于非电解质的是( )
| A. | 铁 | B. | 氯化钙 | C. | 硫酸 | D. | 二氧化碳 |
9.下列有机物分子中所有的原子不可能处于同一平面的是( )
| A. | 1,3-丁二烯 | B. | 乙烷 | C. | 苯乙烯 | D. | 甲醛 |
11.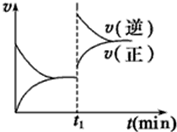 如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )
 如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )| A. | 2SO2(g)+O2(g)?2SO3(g);△H<0 | B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g);△H<0 | ||
| C. | H2(g)+I2(g)?2HI(g);△H>0 | D. | N2(g)+3H2(g)?2 NH3(g)△H<0 |
8.SiCl4的分子结构与CCl4相似,对其进行下列推测,不正确的是( )
| A. | SiCl4晶体是分子晶体 | |
| B. | 常温常压下SiCl4是气体 | |
| C. | SiCl4的分子 是由极性键形成的非极性分子 | |
| D. | SiCl4的熔点高于CCl4 |
12.化学与生产、生活、环境等社会实际密切相关.下列叙述错误的是( )
| A. | 食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需的营养物质 | |
| B. | 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的 | |
| C. | 金属钠具有强的还原性,可利用钠和熔融TiCl4反应制取金属Ti | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生相关 |