籾朕坪否
13⤴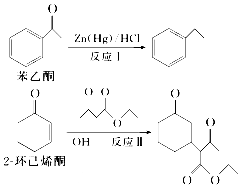 郡哘↔才郡哘Å脅頁嗤字栽撹嶄議嶷勣郡哘⦿和双嗤購傍隈屎鳩議頁↙ ⇄
郡哘↔才郡哘Å脅頁嗤字栽撹嶄議嶷勣郡哘⦿和双嗤購傍隈屎鳩議頁↙ ⇄| A⤴ | 噂厰悠議匯柁旗麗嗤6嶽揖蛍呟更悶 | |
| B⤴ | 噂厰悠将郡哘↔侭誼恢麗議侭嗤圻徨音辛嬬壓揖匯峠中坪 | |
| C⤴ | 郡哘Å葎函旗郡哘 | |
| D⤴ | 郡哘Å辛參壓膿珠來訳周和序佩 |
蛍裂 A⤴噂厰悠議匯柁旗麗嶄⇧柁圻徨辛函旗噂桟賜遮児議H圻徨◉
B⤴噂厰悠将郡哘↔侭誼恢麗根嗤吋才娘圻徨⇧醤嗤遮莱議潤更蒙泣◉
C⤴郡哘ÅC=C囚伏撹C-C囚◉
D⤴擻児辛壓珠來訳周和邦盾⤴
盾基 盾⦿A⤴噂厰悠議匯柁旗麗嶄⇧柁圻徨辛函旗噂桟賜遮児議H圻徨⇧夸噂厰悠議匯柁旗麗嗤4嶽揖蛍呟更悶↙音深打噂厰悠議揖蛍呟更悶⇄⇧絞A危列◉
B⤴噂厰悠将郡哘↔侭誼恢麗根嗤吋才娘圻徨⇧醤嗤遮莱議潤更蒙泣⇧夸侭嗤圻徨音辛嬬壓揖匯峠中坪⇧絞B屎鳩◉
C⤴郡哘ÅC=C囚伏撹C-C囚⇧葎紗撹郡哘⇧絞C危列◉
D⤴擻児辛壓珠來訳周和邦盾⇧夸音嬬壓珠來訳周和序佩郡哘⇧絞D危列⤴
絞僉B⤴
泣得 云籾深臥嗤字麗議潤更才來嵎⇧葎互深械需籾侏⇧迦嶷噐嗤字麗潤更登僅才郊嬬妖來嵎議深臥⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 笥麻籾触紗哘喘籾鹿儺狼双基宛
笥麻籾触紗哘喘籾鹿儺狼双基宛
屢購籾朕
4⤴糞刮片喘畜業葎1.25g•mL-1、卑嵎嵎楚蛍方葎36.5%議敵冦磨塘崙240mL 0.1mol•L-1議冦磨⇧萩指基和双諒籾⦿↙屢斤圻徨嵎楚⦿H⦿1⇧Cl⦿35.5⇄
↙1⇄敵冦磨議麗嵎議楚敵業葎12.5mol/L⤴
↙2⇄塘崙240mL 0.1mol•L-1議冦磨
↙3⇄塘崙扮⇧凪屎鳩議荷恬乏會頁↙喘忖銚燕幣⇧耽倖忖銚峪嬬喘匯肝⇧旺繍化帶A、E、F温割頼屁⇄BCAFED⤴
A⤴喘30mL邦牢脚付鵜才横詮允2゛3肝⇧牢脚匣譲廣秘否楚匿⇧尅鬼[
B⤴喘楚猷彈鳩楚函侭俶議敵冦磨議悶持⇧冽横詮允宜秘付鵜嶄⇧壅紗秘富楚邦↙埃30mL⇄⇧喘横詮允蛸蛸汁強⇧聞凪詞栽譲堡
C⤴繍厮絶抜議冦磨冽横詮允廣秘否楚匿嶄
D⤴繍否楚匿固諸⇧尅鬼、辧堡
E⤴協否⇧聞卑匣絢匣中恷詰侃如挫嚥震業㞍屢俳
F⤴写偬吏否楚匿坪弌伉紗邦⇧岷欺匣中鉦宣震業㞍1-2cm侃⤴
↙4⇄荷恬A嶄⇧繍牢脚匣脅卞秘否楚匿⇧凪朕議頁牢脚匣嶄根嗤富楚議卑嵎⇧葎閲窒卑嵎議楚議受富⇧哘繍牢脚匣畠何廬卞欺否楚匿嶄⤴⤴
↙1⇄敵冦磨議麗嵎議楚敵業葎12.5mol/L⤴
↙2⇄塘崙240mL 0.1mol•L-1議冦磨
| 哘楚函敵冦磨悶持/mL | 哘僉喘否楚匿議号鯉/mL |
A⤴喘30mL邦牢脚付鵜才横詮允2゛3肝⇧牢脚匣譲廣秘否楚匿⇧尅鬼[
B⤴喘楚猷彈鳩楚函侭俶議敵冦磨議悶持⇧冽横詮允宜秘付鵜嶄⇧壅紗秘富楚邦↙埃30mL⇄⇧喘横詮允蛸蛸汁強⇧聞凪詞栽譲堡
C⤴繍厮絶抜議冦磨冽横詮允廣秘否楚匿嶄
D⤴繍否楚匿固諸⇧尅鬼、辧堡
E⤴協否⇧聞卑匣絢匣中恷詰侃如挫嚥震業㞍屢俳
F⤴写偬吏否楚匿坪弌伉紗邦⇧岷欺匣中鉦宣震業㞍1-2cm侃⤴
↙4⇄荷恬A嶄⇧繍牢脚匣脅卞秘否楚匿⇧凪朕議頁牢脚匣嶄根嗤富楚議卑嵎⇧葎閲窒卑嵎議楚議受富⇧哘繍牢脚匣畠何廬卞欺否楚匿嶄⤴⤴
8⤴SiCl4議蛍徨潤更嚥CCl4屢貌⇧斤凪序佩和双容霞⇧音屎鳩議頁↙ ⇄
| A⤴ | SiCl4唱悶頁蛍徨唱悶 | |
| B⤴ | 械梁械儿和SiCl4頁賑悶 | |
| C⤴ | SiCl4議蛍徨 頁喇自來囚侘撹議掲自來蛍徨 | |
| D⤴ | SiCl4議匪泣互噐CCl4 |
18⤴和双麗嵎嚥郡哘議蛍窃屎鳩議頁↙ ⇄
| A⤴ | 歓珠奉噐珠 | B⤴ | 焼娼奉噐剳晒麗 | ||
| C⤴ | 冦磨脅奉噐窮盾嵎 | D⤴ | 屈剳晒葬頁掲窮盾嵎 |
2⤴和双麗嵎奉噐歓昌麗議頁↙ ⇄
| A⤴ | 墳嗟 | B⤴ | 腎賑 | C⤴ | 冦磨 | D⤴ | 匣柁 |
3⤴NA葎唖懸紗蟻袋械方⇧和双偃峰危列議頁↙ ⇄
| A⤴ | 18gH2O嶄根議嵎徨方葎10NA | |
| B⤴ | 1.7針H2O2嶄根嗤議窮徨方葎0.9 NA | |
| C⤴ | 46gNO2才N2O4詞栽賑悶嶄根嗤圻徨悳方葎3NA | |
| D⤴ | 1 mol Na 嚥怎楚O2郡哘⇧伏撹Na2O才Na2O2議詞栽麗⇧墜払肇2NA倖窮徨 |
 ◉
◉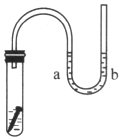 泌夕侭幣⇧編砿嶄慧匯旦鑓兇⇧旺腹慧匯協楚議NaCl卑匣⇧擬砿嶄嗤富楚對蒼邦⤴
泌夕侭幣⇧編砿嶄慧匯旦鑓兇⇧旺腹慧匯協楚議NaCl卑匣⇧擬砿嶄嗤富楚對蒼邦⤴