题目内容
17.下面是利用盐桥电池从某些含碘盐中提取碘的两个装置,下列说法中正确的是( )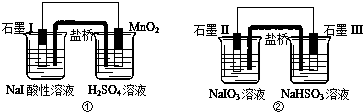
| A. | 两个装置中石墨I和石墨II作负极 | |
| B. | 碘元素在装置①中被氧化,在装置②中被还原 | |
| C. | ①中MnO2的电极反应式为:MnO2+2H2O+2e-═Mn2++4OH? | |
| D. | 反应①、②中生成等量的I2时导线上通过的电子数之比为1:5 |
分析 A、装置①中碘离子失去电子,石墨I为负极;装置②中碘酸钠得电子石墨II作正极;
B、装置①中碘离子失去电子,被氧化;在装置②中碘酸钠得电子被还原;
C、酸性介质中不可能生成氢氧根离子;
D、装置①中碘离子失去电子,1mol碘化钠失去1mol电子;装置②中碘酸钠得电子,1mol碘酸钠得到5mol的电子.
解答 解:A、装置①中碘离子失去电子,石墨I为负极;装置②中碘酸钠得电子石墨II作正极,所以两个装置中石墨I负极而石墨II作正极,故A错误;
B、装置①中碘离子失去电子,被氧化;在装置②中碘酸钠得电子被还原,故B正确;
C、酸性介质中不可能生成氢氧根离子,所以电极反应式为:MnO2+4H++2e-═Mn2++2H2O,故C错误;
D、装置①中碘离子失去电子,1mol碘化钠失去1mol电子;装置②中碘酸钠得电子,1mol碘酸钠得到5mol的电子,所以反应①、②中生成等量的I2时导线上通过的电子数之比为1:5,故D正确;
故选BD.
点评 本题考查化学电源的工作原理,题目难度不大,注意电极反应方程式的书写和判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.若用过量的纯锌粒与一定量的稀硫酸反应,为了加快反应速率又不影响产生氢气的量,下列措施可行的是( )(填序号).
| A. | 微热 | B. | 加入适量氧化铜 | ||
| C. | 加入少量硫酸铜溶液 | D. | 加水 | ||
| E. | 加入少量氢氧化钡溶液 |
5.光导纤维的主要成分是SiO2,对于它的分类中正确的是( )
| A. | 酸性氧化物 | B. | 电解质 | C. | 离子化合物 | D. | 有机物 |
2.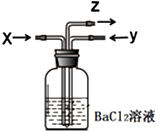 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )| A. | 洗气瓶中产生的沉淀是BaCO3 | B. | Z导管出来的气体中无CO2 | ||
| C. | 洗气瓶中产生的沉淀只有BaSO4 | D. | 洗气瓶中产生的沉淀可能有BaSO3 |
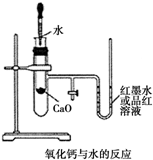 如图是某同学设计的放热反应的观察装置,其实验操作步骤如下:
如图是某同学设计的放热反应的观察装置,其实验操作步骤如下: 如图是实验室制 Cl2 的装置图.
如图是实验室制 Cl2 的装置图.