题目内容
7.W、X、Y、Z均为短周期主族元素,原子序数依次增大,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )| A. | 原子半径:W>X | B. | 氧化物的水化物的酸性:Y<Z | ||
| C. | 阴离子的还原性:W>Z | D. | X与Y不能存在于同一离子化合物中 |
分析 W、X、Y、Z均为的短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,则W是H元素,X是N元素,Y、Z为第三周期元素;
它们的最外层电子数之和为18,W最外层电子数是1,X最外层电子数是5,Y、Z最外层电子数之和是12,且二者都是主族元素,Y原子序数小于Z,则Y是P元素、Z是Cl元素,以此解答该题.
解答 解:W、X、Y、Z均为的短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,则W是H元素,X是N元素,Y、Z为第三周期元素;
它们的最外层电子数之和为18,W最外层电子数是1,X最外层电子数是5,Y、Z最外层电子数之和是12,且二者都是主族元素,Y原子序数小于Z,则Y是P元素、Z是Cl元素,
A.W为H元素,在周期表中原子半径最小,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性P<Cl,最高价氧化物的水化物酸性H3PO4<HClO4,但氧化物的水化物的酸性不一定存在此规律,如磷酸酸性大于次氯酸,故B错误;
C.元素的非金属性越强,其简单阴离子的还原性越弱,非金属性W<Z,所以阴离子的还原性:W>Z,故C正确;
D.X、Y分别是N、P元素,可能存在磷酸铵、磷酸一氢铵、磷酸二氢铵中,磷酸铵、磷酸一氢铵、磷酸二氢铵都是铵盐,属于离子化合物,故D错误;
故选C
点评 本题考查原子结构和元素性质,为高频考点,涉及离子化合物判断、酸性强弱判断、物质熔沸点高低判断、元素周期律等知识点,正确判断元素是解本题关键,结合物质的结构性质解答,易错选项是B.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
15.下列有关NA的说法正确的是( )
| A. | 标准状况下,22.4L SO3中含有的分子数为NA个 | |
| B. | 2L 0.5 mol•L-1亚硫酸溶液中含有的H+离子数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2mol NO和1mol O2充分反应,产物的分子数为2NA |
2.下列物质中,含有共价键的是( )
| A. | KCl | B. | CaO | C. | CO2 | D. | NaCl |
12.将K、SiO2、Na2O、NaOH、NaHSO4分别加热熔化,需要克服相同类型作用力的物质有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
19.有科学家提出,硅是“21世纪的能源”,下面有关硅的叙述中,正确的是( )
| A. | 高纯硅可用于制造光导纤维 | |
| B. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 | |
| C. | 硅的化学性质不活泼,在自然界中可以以游离态存在 | |
| D. | 硅在电子工业中,是重要的半导体材料 |
16.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
| A. |  制乙酸乙酯 | B. |  制氢氧化亚铁 | C. |  石油的蒸馏 | D. |  实验室制乙烯 |
17.下列说法中,不正确的是( )
| A. | 化学是以实验为基础的自然科学 | |
| B. | 化学是一门创造性的、实用性的科学 | |
| C. | 人类的化学实践活动起始于近代 | |
| D. | 现代化学,可称之为21世纪的中心科学 |
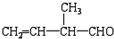 中含氧官能团的结构简式是-CHO;该有机物发生加聚反应后,所得产物的结构简式为
中含氧官能团的结构简式是-CHO;该有机物发生加聚反应后,所得产物的结构简式为 .
.