题目内容
19.有科学家提出,硅是“21世纪的能源”,下面有关硅的叙述中,正确的是( )| A. | 高纯硅可用于制造光导纤维 | |
| B. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 | |
| C. | 硅的化学性质不活泼,在自然界中可以以游离态存在 | |
| D. | 硅在电子工业中,是重要的半导体材料 |
分析 硅为亲氧元素,在自然界中以化合态存在,工业用碳和二氧化硅发生置换反应得到粗硅,硅为重要的半导体材料,为有开发价值的燃料,以此解答该题.
解答 解:A.制作光导纤维的材料为二氧化硅,故A错误;
B.地壳中的含量最高的元素为氧,故B错误;
C.硅为亲氧元素,在自然界中以化合态存在,故C错误;
D.硅具有导电性,为重要的半导体材料,故D正确.
故选D.
点评 本题考查硅的性质,为高频考点,侧重于学生的双基的考查,注意相关基础知识的积累,难度不大,注意硅的性质与用途

练习册系列答案
相关题目
18.已知离子氧化性Fe3+>Cu2+>Fe2+>Zn2+在溶有Fe2(SO4)3和CuSO4的溶液中加入锌粉,下列说法中不正确的是( )
| A. | 若锌粉有剩余,则不溶物中一定有铜,可能有铁 | |
| B. | 若锌粉有剩余,则溶液中的金属阳离子只有Zn2+ | |
| C. | 若锌粉无剩余,且溶液中尚存有Cu2+,则一定有Fe2+ | |
| D. | 若锌粉无剩余,且溶液中无Cu2+,则一定有Zn2+,一定无Fe3+,但不能确定有无Fe2+ |
10.下列试剂不能鉴别CO2和SO2的是( )
| A. | 澄清石灰水 | B. | 品红溶液 | ||
| C. | 酸性高锰酸钾溶液 | D. | 溴水 |
7.W、X、Y、Z均为短周期主族元素,原子序数依次增大,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )
| A. | 原子半径:W>X | B. | 氧化物的水化物的酸性:Y<Z | ||
| C. | 阴离子的还原性:W>Z | D. | X与Y不能存在于同一离子化合物中 |
14.下列实验过程中产生沉淀的物质的量(Y)与加入试剂的量(X)之间的关系正确的是( )
| A. | 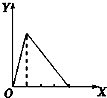 向NaOH溶液中逐滴加入AlCl3溶液至过量且边滴边振荡 | |
| B. | 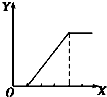 向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡 | |
| C. | 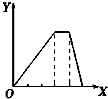 向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量 | |
| D. | 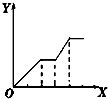 向NaOH、Ba(OH)2、NaA1O2的混合溶液中逐渐通入二氧化碳至过量 |
11.下列元素中不属于主族元素的是( )
| A. | 磷 | B. | 铁 | C. | 碳 | D. | 氧 |
8.下列物质的保存方法正确的是( )
| A. | 用橡皮塞把液溴密封于玻璃瓶中 | |
| B. | 用磨口玻璃塞把氢氟酸密封于棕色试剂瓶中 | |
| C. | 把氯气加压液化后密封于钢瓶中 | |
| D. | 氯水通常保存于无色试剂瓶中 |
9.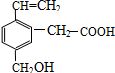 某有机物的结构为图所示,这种有机物具有的性质是( )
某有机物的结构为图所示,这种有机物具有的性质是( )
①可以燃烧;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能发生加聚反应.
 某有机物的结构为图所示,这种有机物具有的性质是( )
某有机物的结构为图所示,这种有机物具有的性质是( )①可以燃烧;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能发生加聚反应.
| A. | ①②④ | B. | ①②③④ | C. | ②③④⑤ | D. | ①②③④⑤ |