题目内容
13.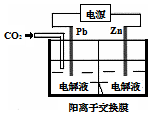 采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )| A. | Pb与电源的正极相连 | |
| B. | ZnC2O4在离子交换膜右侧生成 | |
| C. | 正极反应式为:Zn-2e-═Zn2+ | |
| D. | 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子 |
分析 采用电化学法还原CO2制备ZnC2O4的过程中,碳元素的化合价降低,所以通入二氧化碳的电极是阴极,即Pb是阴极,和电源的负极相连,Zn是阳极,和电源的正极相连,总反应为:2C02+Zn$\frac{\underline{\;通电\;}}{\;}$ZnC2O4,根据反应式计算.
解答 解:A、采用电化学法还原CO2制备ZnC2O4的过程中,碳元素的化合价降低,所以通入二氧化碳的电极是阴极,即Pb是阴极,和电源的负极相连,故A错误;
B、在阴极上,二氧化碳得电子得C2O42-,在阳极上,金属锌失电子成为锌离子,从阳极移向阴极,所以ZnC2O4在交换膜左侧生成,故B错误;
C、Zn是阳极不是正极,金属锌失电子成为锌离子,反应式为:Zn-2e-═Zn2+,故C错误;
D、电解的总反应为:2C02+Zn$\frac{\underline{\;通电\;}}{\;}$ZnC2O4,2mol二氧化碳反应伴随2mol电子转移,当通入标况下的11.2 L CO2时,转移0.5 mol电子,故D正确.
故选D
点评 本题考查学生电解池的工作原理以及电极反应式的书写和应用知识,注意知识的迁移应用是关键,难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
4. 向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
 向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )| A. | 溶液pH:b>c>a | |
| B. | a点:c(H+)-c(OH-)=$\frac{1}{2}$[c(CH3COO-)-c(CH3COOH)] | |
| C. | a到b,溶液中可能存在:c(CH3COO-)=c(Na+) | |
| D. | b到c,溶液中可能存在:c(CH3COO-)=c(OH-) |
5.下列分子中既有σ键又有π键的是( )
| A. | H2O | B. | CH4 | C. | H2 | D. | CO2 |
2.某小组以石膏(CaSO4•2H2O)为主要原料制备(NH4)2SO4的流程如图: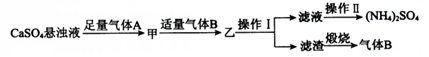
下列说法正确的是( )
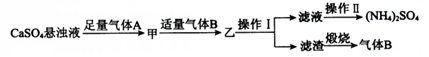
下列说法正确的是( )
| A. | 气体B是NH3,可循环利用 | |
| B. | 操作Ⅰ中,所用的主要玻璃仪器为烧杯、玻璃棒、分液漏斗 | |
| C. | 操作Ⅱ中,可用蒸发结晶的方法得到纯净的(NH4)2SO4 | |
| D. | 整个过程的总反应方程式为CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4 |
9.化学与生活密切相关,下列说法不正确的是( )
| A. | Ge(32号元素)的单晶可以作为光电转换材料用于太阳能电池 | |
| B. | 交警检查司机是否酒后驾车的原理中体现了乙醇的还原性 | |
| C. | 在家用电热水器不锈钢内胆镶嵌镁棒,以防止内胆被腐蚀 | |
| D. | 施用适量石灰乳可降低盐碱地(含较多NaCl、Na2CO3)的碱性 |
17.X、Y、Z、W均为短周期主族元素,原子序数依次递增.X与Z位于同一主族,Z的核外电子数是X的2倍,Y、Z、W原子的最外层电子数之和等于Z的核外电子总数.下列说法正确的是( )
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | Z的最高价氧化物对应的水化物为弱酸 | |
| C. | 在一定条件下,与Y同主族的短周期元素某单质可以与氧化铁发生置换反应 | |
| D. | 常温下,0.1mol•L-1 W的氢化物水溶液的pH>1 |
4.下列实验方案能达到实验目的是( )
| A. | 证明浓度的改变可导致平衡移动:将少量KCl晶体加入FeCl3+3KSC?Fe(SCN)3+3KCl的平衡体系中 | |
| B. | 除去MgCl2溶液中少量的FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量的Mg(OH)2粉末,搅拌一段时间后过滤 | |
| C. | 检验某溶液中是否含有乙醛:向盛有2mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热 | |
| D. | 证明Fe3+的氧化性大于I2:将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 |
20.下列说法不正确的是( )
| A. | 溴被称为“海洋元素” | B. | 硅酸钠可作建筑行业的黏合剂 | ||
| C. | 碳酸钠可作治疗胃酸过多的药剂 | D. | 镁可用于制造信号和焰火 |
1.根据下列实验操作和现象所得出的结论错误的是( )
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有剌激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
| C | 铝片先用砂纸打磨,再加入 到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| D | 向等浓度的KC1、KI混合液中逐滴满加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp (AgI) |
| A. | A | B. | B | C. | C | D. | D |