题目内容
9.化学与生活密切相关,下列说法不正确的是( )| A. | Ge(32号元素)的单晶可以作为光电转换材料用于太阳能电池 | |
| B. | 交警检查司机是否酒后驾车的原理中体现了乙醇的还原性 | |
| C. | 在家用电热水器不锈钢内胆镶嵌镁棒,以防止内胆被腐蚀 | |
| D. | 施用适量石灰乳可降低盐碱地(含较多NaCl、Na2CO3)的碱性 |
分析 A.Ge是32号元素,位于金属和非金属交界线处,可以作半导体材料;
B.重铬酸钾与乙醇反应乙醇作还原剂;
C.作原电池正极的金属被保护;
D.石灰乳为氢氧化钙,氢氧化钙呈碱性.
解答 解:A.32号元素Ge位于金属和非金属交界线处,具有金属和非金属的性质,可以作半导体材料,所以Ge(32号元素)的单晶可以作为光电转换材料用于太阳能电池,故A正确;
B.交警检查司机是否酒后驾车,是用含有重铬酸钾溶液的仪器,重铬酸钾与乙醇反应乙醇作还原剂,体现了乙醇的还原性,故B正确
C.镁、不锈钢和电解质溶液构成原电池,镁易失电子作负极,不锈钢为正极,正极金属被保护,故C正确;
D.氢氧化钙为碱,盐碱地中碳酸钠溶液呈碱性,氢氧化钙和碳酸钠反应生成氢氧化钠,导致盐碱地碱性增强,故D错误;
故选D.
点评 本题考查了化学与生活,明确物质的性质是解本题关键,运用化学知识解释生活现象,学以致用,难度不大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
19. 常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )
常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )
 常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )
常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )| A. | 从图象中可知H2A为强酸 | |
| B. | 当V(NaOH)=20 mL时,溶液中各离子浓度的大小顺序为c(Na+)>c(HA-)>c(H+)>c( A2-)>c(OH-) | |
| C. | 当V(NaOH)=20 mL时混合溶液的pH值大于7 | |
| D. | 当V(NaOH)=40 mL时,升高温度,c(Na+)/c(A2-)减小 |
17.下列实验操作和现象所得结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向等物质的量浓度的NaNO3溶液和Na2SiO3溶液中分别滴加3滴酚酞溶液 | NaNO3溶液为无色,Na2SiO3溶液变成红色 | 非金属性:N>Si |
| B | 将湿润的KI-淀粉试纸置于集满某气体的集气瓶口 | 试纸变蓝 | 该气体为Cl2 |
| C | 将浓盐酸滴入NaHSO3溶液,所得气体依次通过浓硫酸和CuSO4,收集气体 | CuSO4颜色未发生改变 | 收集到纯净的SO2 |
| D | 向含有少量FeCl3的FeCl2溶液中加入铜粉 | 铜粉有剩余 | 所得溶液中的溶质只有FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
4. 乙苯(
乙苯(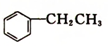 )在有机合成中占有重要的地位,有着广泛的用途.
)在有机合成中占有重要的地位,有着广泛的用途.
已知:①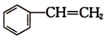 (g)+HCl(g)?
(g)+HCl(g)? (g)△H1=-54kJ•mol-1
(g)△H1=-54kJ•mol-1
②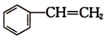 (g)+H2(g)?
(g)+H2(g)?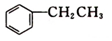 (g)△H2=-121kJ•mol-1
(g)△H2=-121kJ•mol-1
③H2(g)+Cl2(g)═2HCl(g),△H3=-185kJ•mol-1
④相关化学键的键能数据如表所示:
请回答:
(1)根据化学反应原理,缩小容器容积对反应②的影响为缩小容器容积反应速率加快,平衡正向进行,反应物转化率增大;
(2)根据反应①和表中数据计算,x=615;
(3)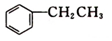 (g)+Cl2(g)?
(g)+Cl2(g)? (g)+HCl(g)△H4
(g)+HCl(g)△H4
①△H4=-118KJ/mol;
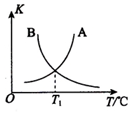
②该反应正、逆反应平衡常数与温度的关系如图所示,其中表示正反应平衡常数K正的曲线为B(填“A”或“B”),理由为反应正反应为放热反应,升温平衡逆向进行平衡常数减小;
③T1℃时,该反应的平衡常数K=1,该温度下,起始向容积为10L的容积可变的密闭容器中充入1mol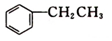 (g)、2mol Cl2(g)、1mol
(g)、2mol Cl2(g)、1mol  (g)、2mol HCl(g),则开始时,v正=(填“>”、“<”或“=”)v逆.
(g)、2mol HCl(g),则开始时,v正=(填“>”、“<”或“=”)v逆.
 乙苯(
乙苯(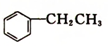 )在有机合成中占有重要的地位,有着广泛的用途.
)在有机合成中占有重要的地位,有着广泛的用途.已知:①
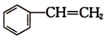 (g)+HCl(g)?
(g)+HCl(g)? (g)△H1=-54kJ•mol-1
(g)△H1=-54kJ•mol-1②
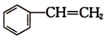 (g)+H2(g)?
(g)+H2(g)?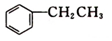 (g)△H2=-121kJ•mol-1
(g)△H2=-121kJ•mol-1③H2(g)+Cl2(g)═2HCl(g),△H3=-185kJ•mol-1
④相关化学键的键能数据如表所示:
| 化学键 | C-H | C-C | C=C | C-Cl | H-Cl |
| 键能/(kJ•mol-1) | 412 | 348 | X | 341 | 432 |
(1)根据化学反应原理,缩小容器容积对反应②的影响为缩小容器容积反应速率加快,平衡正向进行,反应物转化率增大;
(2)根据反应①和表中数据计算,x=615;
(3)
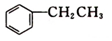 (g)+Cl2(g)?
(g)+Cl2(g)? (g)+HCl(g)△H4
(g)+HCl(g)△H4①△H4=-118KJ/mol;
②该反应正、逆反应平衡常数与温度的关系如图所示,其中表示正反应平衡常数K正的曲线为B(填“A”或“B”),理由为反应正反应为放热反应,升温平衡逆向进行平衡常数减小;
③T1℃时,该反应的平衡常数K=1,该温度下,起始向容积为10L的容积可变的密闭容器中充入1mol
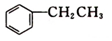 (g)、2mol Cl2(g)、1mol
(g)、2mol Cl2(g)、1mol  (g)、2mol HCl(g),则开始时,v正=(填“>”、“<”或“=”)v逆.
(g)、2mol HCl(g),则开始时,v正=(填“>”、“<”或“=”)v逆.
13.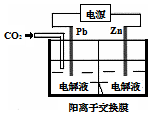 采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
 采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )| A. | Pb与电源的正极相连 | |
| B. | ZnC2O4在离子交换膜右侧生成 | |
| C. | 正极反应式为:Zn-2e-═Zn2+ | |
| D. | 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子 |
19.在给定条件下,下列选项中物质间的转化均能一步实现的是( )
| A. | S$\stackrel{O_{2}}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | Al3+$\stackrel{过量氨水}{→}$AlO${\;}_{2}^{-}$$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| C. | NaCl(aq)$\stackrel{电解}{→}$Na$\stackrel{O_{2}}{→}$Na2O2 | |
| D. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq) $\stackrel{NaOH(aq)}{→}$Fe(OH)2 |
16.常温下,下列有关电解成溶液的说法正确的是( )
| A. | pH=2的H2SO4与pH=12的NaOH等体积混合,所得溶液呈酸性 | |
| B. | 0.1mol/L的CH3COOH溶液在加水稀释过程中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$减小 | |
| C. | pH=5的NaHSO4溶液中水的电离程度小于纯水的电离程度 | |
| D. | 0.1mol/L的NaHCO3溶液中:c(OH-)═(H+)+2c(H2CO3)+c(HCO3-) |
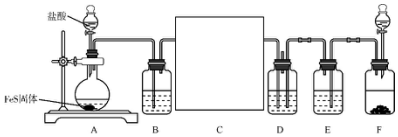


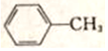 ,G的名称是苯甲醛.
,G的名称是苯甲醛.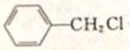 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$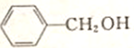 +NaCl.
+NaCl. .
. 以物质的量之比2:1反应得到化合物的结构简式为
以物质的量之比2:1反应得到化合物的结构简式为 .
.