题目内容
4. 向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )| A. | 溶液pH:b>c>a | |
| B. | a点:c(H+)-c(OH-)=$\frac{1}{2}$[c(CH3COO-)-c(CH3COOH)] | |
| C. | a到b,溶液中可能存在:c(CH3COO-)=c(Na+) | |
| D. | b到c,溶液中可能存在:c(CH3COO-)=c(OH-) |
分析 A.向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,随着氢氧化钠的增多,氢离子浓度逐渐减小;
B.a点:溶液中溶质为等物质的量浓度的CH3COOH和CH3COONa,根据物料守恒和电荷守恒分析;
C.溶液显中性时,c(CH3COO-)=c(Na+);
D.c点溶质为等物质的量浓度的NaOH和CH3COONa,结合CH3COONa的水解判断.
解答 解:A.向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,随着氢氧化钠的增多,氢离子浓度逐渐减小,则溶液的pH逐渐增大,即溶液pH为c>b>a,故A错误;
B.a点:溶液中溶质为等物质的量浓度的CH3COOH和CH3COONa,溶液中电荷守恒为c(CH3COO-)+c(OH-)=c(Na+)+c(H+),物料守恒为2c(Na+)=c(CH3COO-)+c(CH3COOH),则c(H+)-c(OH-)=$\frac{1}{2}$[c(CH3COO-)-c(CH3COOH)],故B正确;
C.溶液中电荷守恒为c(CH3COO-)+c(OH-)=c(Na+)+c(H+),溶液显中性时c(H+)=c(OH-),则c(CH3COO-)=c(Na+),故C正确;
D.c点溶质为等物质的量浓度的NaOH和CH3COONa,由于CH3COO-发生水解,则c(CH3COO-)<c(OH-),减少氢氧化钠的量时,溶液中可能存在:c(CH3COO-)=c(OH-),故D正确.
故选A.
点评 本题考查酸碱混合微粒大小比较等,侧重考查醋酸的电离及图象,明确混合溶液中的溶质以及溶液中守恒关系是解答本题的关键,题目难度中等,题目有利于培养学生对基础知识的应用能力.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
12.下列微粒不能破坏水的电离平衡的是( )
| A. | Fˉ | B. | Fe2+ | C. | Na+ | D. | S2- |
19. 常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )
常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )
 常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )
常温下,向20mL 0.2mol/L二元酸H2A溶液中滴加0.2mol/LNaOH溶液,有关微粒物质的量变化如图.下列叙述正确的是( )| A. | 从图象中可知H2A为强酸 | |
| B. | 当V(NaOH)=20 mL时,溶液中各离子浓度的大小顺序为c(Na+)>c(HA-)>c(H+)>c( A2-)>c(OH-) | |
| C. | 当V(NaOH)=20 mL时混合溶液的pH值大于7 | |
| D. | 当V(NaOH)=40 mL时,升高温度,c(Na+)/c(A2-)减小 |
9.下列说法或化学用语表达正确的是( )
| A. | s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 | |
| B. | p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道也在增多 | |
| C. | 某原子的电子排布式为1s22s2 2p63s2 3p63d54s1属于激发态 | |
| D. | Fe2+的电子排布式为1s22s2 2p63s2 3p63d6 |
16.已知短周期主族元素X、Y、Z、W、R五种元素,原子序数依次增大,X元素的原子是所有元素中原子半径最小的,Y、W同主族,Z、W同周期.X与Y可形成具有18个电子的化合物G,在酸性条件下,在含W阴离子的溶液中加入G可得到W单质.Z是同周期中金属性最强的元素.下列说法不正确的是( )
| A. | 原子半径:X<Y<W<R<Z | |
| B. | 由Y、Z元素可形成两种离子化合物其阳离子与阴离子物质的量之比都是2:1 | |
| C. | 沸点:X2Y>X2W | |
| D. | w与R可形成共价化合物WR2,且WR2是极性分子 |
13.相对分子质量都为88的饱和一元醇与饱和一元羧酸发生酯化反应,最多可得到的酯有(不考虑立体异构)( )
| A. | 18种 | B. | 16种 | C. | 14种 | D. | 12种 |
13.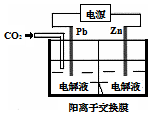 采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
 采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )| A. | Pb与电源的正极相连 | |
| B. | ZnC2O4在离子交换膜右侧生成 | |
| C. | 正极反应式为:Zn-2e-═Zn2+ | |
| D. | 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子 |