��Ŀ����
14��ijУ��ѧ����С������������Һ������������ͭ��ϡ���ᣩ���Ʊ������������岢��������ʵ�飮�Ʊ���������������Ҫ�IJ���������ͼ1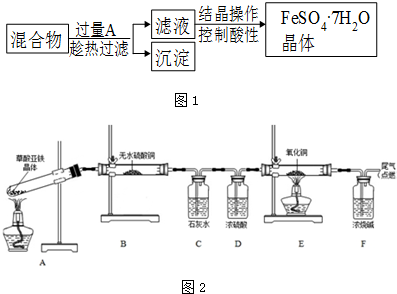
�������ĿҪ��ش��������⣺
��1��A�Ļ�ѧʽΪFe��
��2�����ȹ��˵�Ŀ���Ƿ�ֹ������������������
��3���ᾧ����������Ӧ������Һ���Ե�ԭ��������Fe2+����ˮ�⣮
��4��ʵ�������������������Һ[��NH4��2Fe��SO4��2]�Ͳ�����Һ��Ӧ���ɲ��������������������壨��Է�������180�������ֽ⣬ij����С�������ͼ2��ʵ��װ����������ֽ���
�ٸ�װ����������IJ���A������ĸ����ԭ���Ƿ�Ӧ���ɵ�ˮ�����Թܱ�����ʹ�Թ�ը�ѣ�
�ڸ�����ȷװ�ÿ�ʼʵ�飬B��������˵�����������������нᾧˮ��C���а�ɫ������E����ɫ��ĩ��Ϊ��ɫ��˵�����������ֽ����CO��CO2���ѧʽ����
���� ��1��������������ۣ���Fe3+��Cu2+��H+���ӷ�Ӧת��ΪFe2+��
��2�����ȹ��˵�Ŀ���ǣ�Ҫ����ijЩ�ɷ��ڹ��˹�������������ᾧ�������
��3��Ӧ������ˮ��ĽǶȿ��ǣ���ֹ��������ˮ�������ģ�
��4�����������������ʱ�п�����ˮ��������Aװ�����������Ϊ���Թܹܿ���������б��������ˮ�����ʹ�Թ�ը�ѣ�����B��C��E�жϲ�����H2O����ᾧˮ����CO2��CO������CO�Ĵ���ʹ���������ܴ��ڣ����Dz�����ɫ���壬ӦΪFeO���ݴ˴��⣮
��� �⣺��1��������������ۣ���Fe3+��Cu2+��H+���ӷ�Ӧת��ΪFe2+��
�ʴ�Ϊ��Fe��
��2�����ȹ��˵�Ŀ���ǣ�Ҫ����ijЩ�ɷ��ڹ��˹�������������ᾧ�������
�ʴ�Ϊ����ֹ������������������
��3���������ӿ���ˮ�⣬�ᾧ���������п�����Һ�����ԣ�����������������ˮ�������ģ�
�ʷ���Ϊ������Fe2+����ˮ�⣻
��4���ټ��ȹ���ʱ������ˮ��������Aװ�����������Ϊ���Թܹܿ���������б��������ˮ�����ʹ�Թ�ը�ѣ�
�ʴ�Ϊ��A����Ӧ���ɵ�ˮ�����Թܱ�����ʹ�Թ�ը�ѣ�
�ڸ�����ȷװ�ã�ʵ�鿪ʼ��B������ɫ��˵�����������������нᾧˮ��C���а�ɫ������E�����ֺ�ɫ��ĩ��Ϊ��ɫ��˵�����������ֽ������CO��CO2��CO�Ĵ���ʹ���������ܴ��ڣ����Dz�����ɫ���壬ӦΪFeO��
�ʴ�Ϊ���ᾧˮ��CO��CO2��
���� ��������������������Ʊ�Ϊ���壬��Ҫ�����˳����ᴿ�Ļ�����������ʵ�鲽��ԭ����Ŀ�ķ������ۡ���װ�õķ������۵ȣ���ȷԭ���ǽ���ؼ���Ū���������Ļ�ѧ��Ӧ����Ԫ�ش�����̬�ı仯��

| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
A��CH3COOH+NaCN�TCH3COONa+HCN
B��CO2+H2O+C6H5ONa-��NaHCO3+C6H5OH
C��2HCN+Na2CO3�T2NaCN+CO2+H2O
D��Na2CO3+C6H5OH-��NaHCO3+C6H5ONa
E��CO2+H2O+2NaClO�TNa2CO3+2HClO
����֪HA��H2B���������ᣬ�������¹�ϵ��H2B��������+2A-�TB2-+2HA����A-��B2-��HB-���������ӽ��H+������˳��ΪA-��B2-��HB-��
��2��һЩ���ֽⷴӦ�ķ�������ѭ�������ɣ����б仯�����ڸ��ֽⷴӦ��
�ٽ�ʯ�����봿����Һ��Ͽ��Ƶÿ�������Һ��
����̼�������Һ�м��뱥��ʳ��ˮ�ɻ��С�մ���塡
������KCl��NaNO3�Ļ����Һ����������NaCl���壮
����������Ӧ���ܽ�����ֽⷴӦ��������һ����Ϊ���ܽ����Խϴ�������������ܽ����Խ�С�����ʵķ�����У�
��3��������ij������ܽ���ˮ�к���Һ�е�c��H+��=10-9 mol•L-1����õ���ʿ�����AD������ţ�
A��Na2S B��HCl C��K2SO4 D��NaOH E��CuSO4
��4�������£���pH=3������a L�ֱ�������������Һ��ϣ������Һ�������ԣ�
��Ũ��Ϊ1.0��10-3 mol•L-1�İ�ˮb L��
��c��OH-��=1.0��10-3 mol•L-1�İ�ˮc L��
��c��OH-��=1.0��10-3 mol•L-1������������Һd L��
��a��b��c��d֮���ɴ�С��˳���ǣ�b��a=d��c��
��5��һ���¶��£������������ʵ���Ũ�ȵ�����������Һ����NaOH����CH3COOH����CH3COONa�ֱ�ӵ���ˮ��pH�仯��С���Ǣۣ����ţ���һ���¶��£���������ˮ�зֱ��������ʵ�����CH3COONa��NaCN������Һ�������ӵ������ʵ����ֱ�Ϊn1��n2����n1��n2�Ĺ�ϵΪn1��n2�����������������=������
| A�� | �ڱ����Ȼ�����Һ����μ���NaOH��Һ�������Ƶ�Fe��OH��3���� | |
| B�� | ������������ɢϵ�ı��������ǽ����ܷ��������ЧӦ | |
| C�� | �ð�Ĥ������ۺ�ʳ�εĻ��Һ | |
| D�� | Fe��OH��3��������ϡ���ᣬ��������������ܽ� |
| A�� | ������Ʒ | B�� | ��Ȼ��֬ | C�� | �� | D�� | ������ |
| A�� | ��֪C2H6��ȼ����Ϊ1090 kJ•mol-1����C2H6ȼ�յ��Ȼ�ѧ����ʽΪ��C2H6��g��+3.5O2��g���T2CO2��g��+3H2O��g����H=-1090 kJ/mol | |
| B�� | 25�棬101kPa�£�l mol C6H6ȼ������CO2��Һ̬ˮʱ�ų�3260 kJ���������Ȼ�ѧ����ʽΪ��C6H6��g��+7.5O2��g��=6CO2��g��+3H2O ��l����H=-3260kJ•mol-1 | |
| C�� | ��֪�����£�H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ/mol����ϡ������ϡNaOH��Һ��Ӧ����1 mol H2O��l��ʱҲ�ų�57.3 kJ������ | |
| D�� | ��֪2CO��g��+O2��g���T2CO2��g����H=-566 kJ•mol-1����CO��ȼ���ȡ�H=-283 kJ•mol-1 |
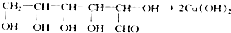 +NaOH$\stackrel{��}{��}$
+NaOH$\stackrel{��}{��}$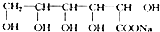 +Cu2O+3H2O��ʵ�����ô˷�����ȡ���������Cu2O���壬��Ҫ�IJ����������Թܡ��ƾ��ơ��ձ�����ͷ�ι��⣬����Ҫ©����������
+Cu2O+3H2O��ʵ�����ô˷�����ȡ���������Cu2O���壬��Ҫ�IJ����������Թܡ��ƾ��ơ��ձ�����ͷ�ι��⣬����Ҫ©����������