题目内容
19.用一定量的二氧化锰与100mL37%的浓盐酸 ( 密度为1.19g/cm3 ) 反应时,收集到2L氯气( 密度为 3.17g/L).求反应剩余物中最多含有氯化氢多少克?分析 根据m=ρV计算生成氯气的质量,根据方程式MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O计算参加反应HCl的质量,结合盐酸密度、质量分数计算溶液中HCl总质量,进而计算剩余HCl的质量.
解答 解:2L 氯气质量为:2L×3.17g/L=6.34g,
设生成 6.34g 氯气需 HCl 的质量为 x,则:
MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
146 71
x 6.34g
即146:71=x:6.34g
解得:x=13.04g
则剩余物中含有氯化氢质量为:100mL×1.19g/mL×37%-13.04g=30.99g,
答:剩余物中含有氯化氢质量为30.99g.
点评 本题考查化学方程式有关计算,比较基础,理解掌握化学方程式的意义.

练习册系列答案
相关题目
7.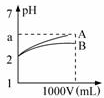 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )| A. | a=5时,A是强酸,B是弱酸 | |
| B. | 若A、B都是强酸,则5>a>2 | |
| C. | 稀释后,A酸溶液的酸性比B酸溶液强 | |
| D. | A、B两种酸溶液的物质的量浓度一定相等 |
4.砹是原子序数最大的卤族元素、根据卤素性质的递变规律,对砹及其化合物的叙述,正确的是( )
| A. | 与H2化合能力:At2>I2 | B. | 砹在常温下为白色固体 | ||
| C. | 砹原子的最外电子层上有7个电子 | D. | 砹能从NaCl溶液中置换出氯单质 |
11.下列有关说法正确的是( )
| A. | 一定条件下反应N2+3H2$?_{加热}^{催化剂}$2NH3,达到平衡时,3v正(H2)=2v正(NH3) | |
| B. | 10mL浓度为1mol/L的盐酸与过量的Zn粉反应,若加入适量的CH3COONa溶液,既能降低反应速率,又不影响H2的生成 | |
| C. | 将pH=a+1的氨水稀释为pH=a的过程中,c(OH-)/c(NH3•H2O)变小 | |
| D. | 常温下,向浓度为0.1mol/L的CH3COONa溶液中加入等体积等浓度的CH3COOH,混合溶液的pH=7 |
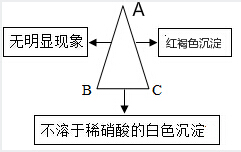 现有A、B、C三种物质,已知A是一种氯化物,B是一种钠盐,C是一种碱,下图表示的是A、B、C的溶液两两混合的实验现象.请回答下列个小题:
现有A、B、C三种物质,已知A是一种氯化物,B是一种钠盐,C是一种碱,下图表示的是A、B、C的溶液两两混合的实验现象.请回答下列个小题: