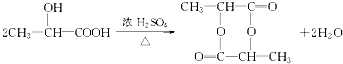��Ŀ����
12��W��R��X��Y��ԭ��������������Y��������ۺ������֮�͵���0��L���ϵ�������M���ϵ�������2�����ڳ��³�ѹ�£�W��R��ɵĻ������ж��֣��������ֻ��������ת������Ԫ�ػ��ϼ�û�б仯����4��Ԫ�ص�ԭ������������֮�͵���Rԭ�ӵĺ˵������2��������˵����ȷ���ǣ�������| A�� | Ԫ�صķǽ�����˳��ΪR��Y��W | |
| B�� | R����������Ԫ�ؾ����γɹ��ۻ����� | |
| C�� | ���⻯������ȶ���˳��ΪR��W��Y | |
| D�� | ԭ�Ӱ뾶����ΪW��R��X��Y |
���� W��R��X��Y��ԭ��������������Y��������ۺ������֮�͵���0����Yλ�ڵ�IVA�壬L���ϵ�������M���ϵ�������2������Y��M������4�����ӣ�ΪSiԪ�أ�
�ڳ��³�ѹ�£�����W��RԪ����ɵ����ֻ�����֮�����ת������ת��������û�л��ϼ۱仯����������������������֮�����ת������û�е���ת�ƣ���WΪN��RΪOԪ�أ���4��Ԫ�ص�����������֮�͵���Rԭ�ӵĺ˵������2����R�˵����Ϊ8��W�������5�����ӡ�R�������6�����ӡ�Y�������4�����ӣ���X�������1����Xԭ����������R��С��Y��ΪNaԪ�أ�Ȼ����Ԫ�ص����ʺ�Ԫ�������������
��� �⣺W��R��X��Y��ԭ��������������Y��������ۺ������֮�͵���0����Yλ�ڵ�IVA�壬L���ϵ�������M���ϵ�������2������Y��M������4�����ӣ�ΪSiԪ�أ�
�ڳ��³�ѹ�£�����W��RԪ����ɵ����ֻ�����֮�����ת������ת��������û�л��ϼ۱仯����������������������֮�����ת������û�е���ת�ƣ���WΪN��RΪOԪ�أ���4��Ԫ�ص�����������֮�͵���Rԭ�ӵĺ˵������2����R�˵����Ϊ8��W�������5�����ӡ�R�������6�����ӡ�Y�������4�����ӣ���X�������1����Xԭ����������R��С��Y��ΪNaԪ�أ���
A��W��R��Y�ֱ���N��O��SiԪ�أ�ͬһ����Ԫ�أ�Ԫ�طǽ���������ԭ�������������ǿ��ͬһ����Ԫ�أ�Ԫ�طǽ���������ԭ��������������������Էǽ�����ǿ��˳����R��W��Y����A����
B�����ý����ͻ��÷ǽ���Ԫ��֮�����γ����ӻ����R�ǻ��÷ǽ���Ԫ�ء�X�ǻ��ý���Ԫ�أ��������γ����ӻ�����Na2O��Na2O2����B����
C��Ԫ�صķǽ�����Խǿ������⻯����ȶ���Խǿ���ǽ�����R��W��Y������⻯������ȶ��Դ���ΪR��W��Y����C��ȷ��
D��ԭ�ӵ��Ӳ���Խ����ԭ�Ӱ뾶Խ��ͬһ����Ԫ�أ�ԭ�Ӱ뾶����ԭ�������������С������ԭ�Ӱ뾶��С˳����X��Y��W��R������D����
��ѡC��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɣ�Ϊ��Ƶ���㣬����ԭ�ӽṹ��ԭ��������ϵ��Ԫ�ػ�����֪ʶ�ƶ�Ԫ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��N�Ļ�����֮���ת������Ŀ�ѶȲ���

| A�� | Cu�������� | B�� | H2SO4�ڷ�Ӧ��ֻ���������� | ||
| C�� | Cu�ڷ�Ӧ�б����� | D�� | 1mol�������ڷ�Ӧ�еõ�1mol���� |
��ij��ֽ���ų��ķ�ˮ����ȡ���������г��˺������빯����ά���Լ��������л����⣬�����ɷ�Ϊc��Na+��=4��10-4mol/L��c��SO42-��=2.5��10-4mol/L��c��Cl-��=1.6��10-5 mol/L��c��NO3-��=1.4��10-5 mol/L��c��Ca2+��=1.5��10-5 mol/L����÷�ˮ��pHΪ4��
��������һԪ��HA��HB��HC��HD����ͬ���ʵ���Ũ�ȵ�NaD��NaB��Һ��pH��ǰ�߱Ⱥ��ߴ�NaA��Һ�����ԣ�1mol/L��KC��Һ����̪��Һ�ʺ�ɫ��ͬ�����ͬ���ʵ���Ũ�ȵ�HB��HC�ֱ������������飬���ֺ��ߵĵ����Ա�ǰ��ǿ�������������������ǿ������˳��ΪHA��HC��HB��HD��
�����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�����
��Һ��pH���±���
| ʵ���� | HA���ʵ���Ũ�ȣ�mol/L�� | NaOH���ʵ���Ũ�ȣ�mol/L�� | �����Һ��pH |
| �� | 0.1 | 0.1 | pH=9 |
| �� | c | 0.2 | pH=7 |
| �� | 0.2 | 0.1 | pH��7 |
��1���Ӣ������������HA��ǿ�ỹ���������ᣨ�ǿ�ᡱ�����ᡱ����
��2������ʵ�����û����Һ����ˮ�������c��OH-��=10-5mol•L-1��
��3���������������c����0.2mol/L��ѡ����ڡ�����С�ڡ����ڡ��������Һ������Ũ��c��A-����c��Na+���Ĵ�С��ϵ��c��A-��=c��Na+����
��4���Ӣ���ʵ����������˵��HA�ĵ���̶ȴ���NaA��ˮ��̶ȣ�ѡ����ڡ�����С�ڡ����ڡ������û����Һ������Ũ���ɴ�С��˳����c��A-����c��Na+����c��H+����c��OH-����
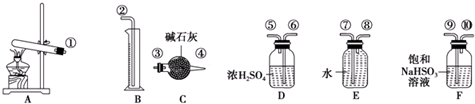
��������롿
����������ijɷֿ���ֻ��SO3һ�֣�
����������ijɷֿ��ܺ���SO2��O2���֣�
����������ijɷֿ��ܺ���SO3��SO2��O2���֣�
��ʵ��̽����
ʵ����������ԣ�
��֪ʵ�����ʱ������ͭ��ȫ�ֽ⣮
��1��������װ̽��ʵ���װ�ã����������ҵķ��������ӿڵ�����˳��Ϊ���١��������ޡ��ݡ��ۡ��ܡ�����ߡ��ڣ���ӿ���ţ���
��2����ʵ�����ʱB����Ͳû���ռ���ˮ����֤���������ȷ��
��3��������ʵ��С����и�ʵ�飬���ڼ���ʱ���¶Ȳ�ͬ��ʵ����������������Ҳ��ͬ���������£�
| ʵ��С�� | ��ȡCuSO4������/g | װ��C���ӵ�����/g | ��Ͳ��ˮ���������ɱ�״������������/mL |
| һ | 6.4 | 2.56 | 448 |
| �� | 6.4 | 2.56 | 224 |
��һС�飺2CuSO4$\frac{\underline{\;\;��\;\;}}{\;}$2CuO+2SO2��+O2����
�ڶ�С�飺4CuSO4$\frac{\underline{\;\;��\;\;}}{\;}$4CuO+2SO2��+2SO3��+O2����
| A�� | 58.5 g���Ȼ��ƹ����к���NA���Ȼ��Ʒ��� | |
| B�� | ��״���£�5.6 Lһ��������5.6 L������Ϻ�ķ�������Ϊ0.5NA | |
| C�� | 0.1 mol•L-1����������Һ�к���������Ϊ0.1NA | |
| D�� | 5.6 g��������ϡ���ᷴӦʱʧȥ������Ϊ0.2NA |
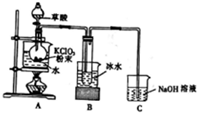 �������ȣ�ClO2����һ�ָ�Ч����������60��ʱ�����������ᣨ��ǿ�ᣩ��Ӧ���Ʊ��������ȣ�ʵ��װ����ͼ��ʾ����֪��ͨ������£��������ȵķе�Ϊ11.0�棬���ױ�ը����ȡ��ʹ�ö�������ʱҪ������ȷ��������ϡ�ͣ��Է���ը���ش��������⣺
�������ȣ�ClO2����һ�ָ�Ч����������60��ʱ�����������ᣨ��ǿ�ᣩ��Ӧ���Ʊ��������ȣ�ʵ��װ����ͼ��ʾ����֪��ͨ������£��������ȵķе�Ϊ11.0�棬���ױ�ը����ȡ��ʹ�ö�������ʱҪ������ȷ��������ϡ�ͣ��Է���ը���ش��������⣺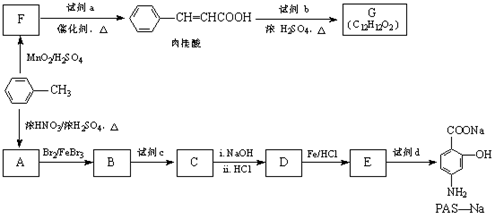
 ��R-CH3��-H��
��R-CH3��-H�� $\stackrel{Fe/HCl}{��}$
$\stackrel{Fe/HCl}{��}$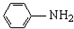
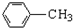 $\stackrel{KMnO_{4}/H+}{��}$
$\stackrel{KMnO_{4}/H+}{��}$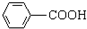
 ����A�ķ�Ӧ������ȡ����Ӧ��
����A�ķ�Ӧ������ȡ����Ӧ��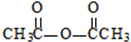 ��
�� ��
��
 �������������
�������������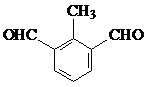 ��
��  ����дһ�ּ��ɣ���
����дһ�ּ��ɣ���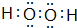 ��
��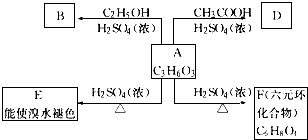
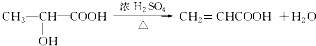 ��A��F
��A��F