题目内容
下列实验操作或装置不符合实验要求的是( )
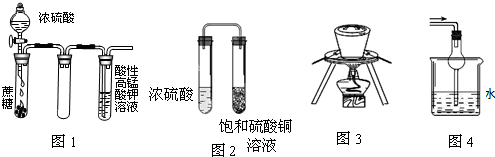

| A、图1酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
| B、图2久置后,饱和硫酸铜溶液可能析出蓝色晶体 |
| C、图3在海带提碘实验中用于灼烧海带 |
| D、图4可用于吸收易溶于水的尾气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.浓硫酸和蔗糖反应生成二氧化碳和二氧化硫气体;
B.浓硫酸具有吸水性;
C.坩埚用于灼烧;
D.球形装置可防止倒吸.
B.浓硫酸具有吸水性;
C.坩埚用于灼烧;
D.球形装置可防止倒吸.
解答:
解:A.浓硫酸和蔗糖反应生成二氧化碳和二氧化硫气体,二氧化硫具有还原性,二氧化碳微溶于水,溶液中有气泡,故A正确;
B.浓硫酸具有吸水性,则久置后,饱和硫酸铜溶液溶剂减少,可能析出蓝色晶体,故B错误;
C.坩埚用于灼烧,则在海带提碘实验中用于灼烧海带,故C错误;
D.球形装置可防止倒吸,则可用于吸收易溶于水的尾气,故D错误;
故选A.
B.浓硫酸具有吸水性,则久置后,饱和硫酸铜溶液溶剂减少,可能析出蓝色晶体,故B错误;
C.坩埚用于灼烧,则在海带提碘实验中用于灼烧海带,故C错误;
D.球形装置可防止倒吸,则可用于吸收易溶于水的尾气,故D错误;
故选A.
点评:本题考查化学实验方案的评价,涉及物质的性质、灼烧、防止倒吸装置及饱和溶液,侧重实验操作的考查,注重基础知识的考查,题目难度不大.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
下列情况不会造成水污染的是( )
| A、工业废水、废物的任意排放 |
| B、农业上大量施用农药和化肥 |
| C、用第四代广谱杀菌消毒剂的ClO2对水进行消毒杀菌 |
| D、生活中大量使用含磷洗衣粉,并把污水随意排放 |
用NA表示阿伏加德罗常数,下列说法中正确的有( )
| A、2.4g金属镁与足量盐酸反应,转移电子的数目为0.1NA |
| B、1mol/L的CaCl2溶液中含Cl-的数目为2NA |
| C、常温常压下,1.7gNH3中含N-H键数目为0.3 NA |
| D、标准状况下,11.2 L H2O含有的电子数为5 NA |
在一定的温度下,将 2mol SO2和1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
| A、生成SO3 2 mol |
| B、放出 197 kJ 的热量 |
| C、SO2 的转化率为100% |
| D、平衡时压强不再改变 |
在下列各溶液中,一定能大量共存的一组离子是( )
| A、含有AlO2-的溶液中:Na+、Al3+、NO3-、Cl- |
| B、使淀粉碘化钾变蓝的溶液中:K+、HCO3-、S2-、SO42- |
| C、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Na+ |
| D、通有SO2的溶液中:Fe2+、Mg2+、Cl-、SO42- |