题目内容
在一定的温度下,将 2mol SO2和1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
| A、生成SO3 2 mol |
| B、放出 197 kJ 的热量 |
| C、SO2 的转化率为100% |
| D、平衡时压强不再改变 |
考点:化学平衡的计算
专题:化学平衡专题
分析:A.可逆反应不能进行到底,反应物不可能100%地全部转化为生成物;
B.2mol SO2和1mol O2完全转化为2molSO3放出的热量为197KJ,可逆反应不能进行到底;
C.可逆反应不能进行到底,反应物不可能100%地全部转化为生成物;
D.2SO2(g)+O2(g)?2SO3(g)是气体体积减小的反应,平衡时各组分的含量不变.
B.2mol SO2和1mol O2完全转化为2molSO3放出的热量为197KJ,可逆反应不能进行到底;
C.可逆反应不能进行到底,反应物不可能100%地全部转化为生成物;
D.2SO2(g)+O2(g)?2SO3(g)是气体体积减小的反应,平衡时各组分的含量不变.
解答:
解:A.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故生成SO3小于2mol,故A错误;
B.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故放出的热量小于197kJ,故B错误;
C.可逆反应不能进行到底,反应物不可能100%地全部转化为生成物,SO2 的转化率小于100%,故C错误;
D.2SO2(g)+O2(g)?2SO3(g)是气体体积减小的反应,平衡时各组分的含量不变,压强不再改变,故D正确.
故选:D.
B.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故放出的热量小于197kJ,故B错误;
C.可逆反应不能进行到底,反应物不可能100%地全部转化为生成物,SO2 的转化率小于100%,故C错误;
D.2SO2(g)+O2(g)?2SO3(g)是气体体积减小的反应,平衡时各组分的含量不变,压强不再改变,故D正确.
故选:D.
点评:本题考查可逆反应的特点,难度不大,要注意可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
现有等浓度的下列溶液:①醋酸,②次氯酸,③碳酸氢钠,④碳酸,⑤碳酸钠.按溶液pH由小到大排列正确的是( )
| A、④①②⑤③ |
| B、④①②③⑤ |
| C、①④②③⑤ |
| D、①④②⑤③ |
高温下,某反应达平衡,平衡常数K=
.恒容时,温度升高,B的浓度减小.下列说法正确的是( )
①该反应的焓变为正值
②恒温恒容下,增大压强,B浓度一定减小
③升高温度,逆反应速率减小
④该反应化学方程式为C(g)+D(g)?A(g)+B(g)
⑤增加A的量,平衡向正反应方向移动
⑥加入催化剂,B的转化率提高.
| c(C)c(D) |
| c(A)c(B) |
①该反应的焓变为正值
②恒温恒容下,增大压强,B浓度一定减小
③升高温度,逆反应速率减小
④该反应化学方程式为C(g)+D(g)?A(g)+B(g)
⑤增加A的量,平衡向正反应方向移动
⑥加入催化剂,B的转化率提高.
| A、①③⑥ | B、①⑤ |
| C、①④⑤ | D、②⑤ |
下列实验操作或装置不符合实验要求的是( )
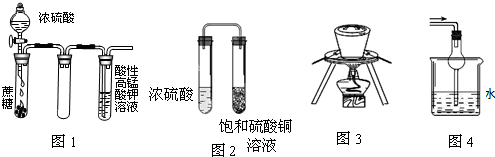

| A、图1酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
| B、图2久置后,饱和硫酸铜溶液可能析出蓝色晶体 |
| C、图3在海带提碘实验中用于灼烧海带 |
| D、图4可用于吸收易溶于水的尾气 |
用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作导致结果偏大的是( )
| A、碱式滴定管用蒸馏水洗净后,直接加入未知浓度的NaOH溶液 |
| B、锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
| C、滴定前,没有逐出酸式滴定管尖嘴处的气泡,滴定终点时气泡消失 |
| D、滴定前读数正确,达到滴定终点后,俯视读数 |