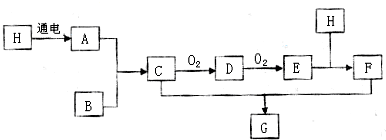
题目内容
19.A为某饱和一元羧酸,8.8g该物质与足量NaHCO3溶液反应生成2.24L CO2(标准状况),则A的分子式为C4H8O2.分析 一元羧酸与碳酸氢钠反应的方程式为CnH2nO2+NaHCO3→CnH2n-1O2Na+CO2↑+H2O,结合反应的方程式计算该题.
解答 解:设A的分子式为CnH2nO2,则有:
CnH2nO2+NaHCO3→CnH2n-1O2Na+CO2↑+H2O
(14n+32)g 22.4L
8.8g 2.24L
则$\frac{(14n+32)g}{8.8g}$=$\frac{22.4L}{2.24L}$,解得n=4,即A的分子式为C4H8O2,
故答案为:C4H8O2.
点评 本题考查有机物分子式的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握反应的关系式,难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
9.在200mL某硫酸盐溶液中含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为( )
| A. | 1 mol•L-1 | B. | 2.5 mol•L-1 | C. | 5 mol•L-1 | D. | 2 mol•L-1 |
10.草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性.向100mL0.2mol/L的草酸溶液中加入1.68 g KOH固体,若溶液体积不变,则对所得溶液中各粒子浓度之间的关系描述错误的是( )
| A. | c(C2O42-)+c(HC2O4-)+c(OH-)=c(K+)+c(H+) | |
| B. | c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.2mol/L | |
| C. | c(C2O42-)<c(HC2O4-)<c(H2C2O4) | |
| D. | c(C2O42-)+c(HC2O4-)+c(H2C2O4)<c(K+) |
8.将PH=1的盐酸平均分成2份,一份加适量水,另一份加入与该盐酸的物质的量浓度相同的NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比约为( )
| A. | 9:2 | B. | 10:1 | C. | 11:1 | D. | 12:1 |
9.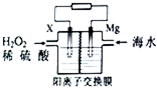 交通运输部在南海华阳礁举行华阳灯塔和赤灯塔竣工发光仪式,宣布两座大型多功能灯塔正式发光并投入使用.灯塔可用镁海水电池提供能源,其装置如图所示.下列有关海水电池的说法正确的是( )
交通运输部在南海华阳礁举行华阳灯塔和赤灯塔竣工发光仪式,宣布两座大型多功能灯塔正式发光并投入使用.灯塔可用镁海水电池提供能源,其装置如图所示.下列有关海水电池的说法正确的是( )
 交通运输部在南海华阳礁举行华阳灯塔和赤灯塔竣工发光仪式,宣布两座大型多功能灯塔正式发光并投入使用.灯塔可用镁海水电池提供能源,其装置如图所示.下列有关海水电池的说法正确的是( )
交通运输部在南海华阳礁举行华阳灯塔和赤灯塔竣工发光仪式,宣布两座大型多功能灯塔正式发光并投入使用.灯塔可用镁海水电池提供能源,其装置如图所示.下列有关海水电池的说法正确的是( )| A. | X可为铁、铜、石墨等电极,发生氧化反应 | |
| B. | 每转移2 mol电子,2molH+由交换膜左侧向右侧迁移 | |
| C. | 该电池能将化学能全部转化成电能 | |
| D. | 正极的电极反应式为比O2+2e-+2H+═2H2O |