题目内容
9.在200mL某硫酸盐溶液中含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为( )| A. | 1 mol•L-1 | B. | 2.5 mol•L-1 | C. | 5 mol•L-1 | D. | 2 mol•L-1 |
分析 硫酸根离子的物质的量=$\frac{1.5{N}_{A}}{{N}_{A}/mol}$=1.5mol,金属阳离子物质的量=$\frac{{N}_{A}}{{N}_{A}/mol}$=1mol,则金属阳离子和硫酸根离子的物质的量之比=1mol:1.5mol=2:3,根据电荷守恒知,金属阳离子带3个单位正电荷,则硫酸盐的物质的量为金属阳离子的一半,则硫酸盐的物质的量为0.5mol,根据C=$\frac{n}{V}$计算硫酸盐的物质的量浓度.
解答 解:硫酸根离子的物质的量=$\frac{1.5{N}_{A}}{{N}_{A}/mol}$=1.5mol,金属阳离子物质的量=$\frac{{N}_{A}}{{N}_{A}/mol}$=1mol,则金属阳离子和硫酸根离子的物质的量之比=1mol:1.5mol=2:3,根据电荷守恒知,金属阳离子带3个单位正电荷,则硫酸盐的物质的量为金属阳离子的一半,则硫酸盐的物质的量为0.5mol,则硫酸盐的物质的量浓度=$\frac{0.5mol}{0.2L}$=2.5mol/L,
故选B.
点评 本题考查物质的量浓度有关计算,为高频考点,侧重考查学生分析计算能力,正确判断阳离子物质的量与硫酸盐的物质的量关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
20.某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol?L-1、0.001mol?L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol?L-1)的用量均为2mL.
(1)请完成以下实验设计表:
(2)某同学对实验①和②分别进行三次实验,测得以下实验数据(从混合振荡均匀开始计时)
计算用0.001 mol?L-1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率1×10-4mol•L-1•min-1(忽略混合前后溶液体积的变化).
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?否.若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应.
(1)请完成以下实验设计表:
| 实验 编号 | T/K | 催化剂的 用量/g | KMnO4酸性溶液 的浓度/mol?L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究催化剂对该反应速率的影响 |
| ② | ||||
| ③ | ||||
| ④ |
| KMnO4酸性溶液的浓度/mol.L-1 | 溶液褪色所需时间t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?否.若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应.
17.下列物质不可能由醛与氢气发生加成反应得到的是( )
| A. | 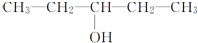 | B. | CH3-CH2-CH2-CH2OH | ||
| C. |  | D. | 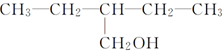 |
4.有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式1s22s22p63s1.
(2)B元素在周期表中的位置第3周期第ⅢA族;简单离子半径:B离子小于C离子(填“大于”或“小于”).
(3)D原子的外围电子排布式为3s23p5.
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应水化物反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,与C的最高价氧化物对应水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式1s22s22p63s1.
(2)B元素在周期表中的位置第3周期第ⅢA族;简单离子半径:B离子小于C离子(填“大于”或“小于”).
(3)D原子的外围电子排布式为3s23p5.
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应水化物反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,与C的最高价氧化物对应水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
14.表是A、B、C、D、E五种有机物的有关信息:
根据表中信息回答下列问题:
(1)A与水在一定条件下反应生成的物质C是乙醇(填名称);写出在一定条件下,A生成高分子化合物的化学方程式:nCH2=CH2$\stackrel{催化剂}{→}$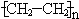 .
.
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤任何条件下不与氢气反应 ⑥可使酸性高锰酸钾溶液和溴水均褪色
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: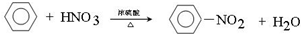 .
.
(4)写出由C氧化生成D的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(5)C与E反应能生成相对分子质量为100的酯,该反应类型为取代(酯化)反应;其化学方程式为:CH2=CH-COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH2=CH-COOC2H5+H2O.
| A | B | C | D | E |
| ①能使溴水褪色 ②比例模型为  ③能与水在一定条件下反应生成物质C | ①由C、H两 种元素组成 ②球棍模型为 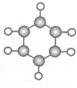 | ①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 ③能与E反应生成相对分子质量为100的酯 | ①相对分子质量 比物质C小2②能由物质C氧化而成 | ①由C、H、O三种元素组成 ②球棍模型为  |
(1)A与水在一定条件下反应生成的物质C是乙醇(填名称);写出在一定条件下,A生成高分子化合物的化学方程式:nCH2=CH2$\stackrel{催化剂}{→}$
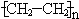 .
.(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤任何条件下不与氢气反应 ⑥可使酸性高锰酸钾溶液和溴水均褪色
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.(4)写出由C氧化生成D的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(5)C与E反应能生成相对分子质量为100的酯,该反应类型为取代(酯化)反应;其化学方程式为:CH2=CH-COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH2=CH-COOC2H5+H2O.
1.设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | 18 g H2O含有3NA个原子 | |
| B. | 1 mol甲苯含有6NA个C-H键 | |
| C. | 标准状况下,22.4 L氯水含有NA个Cl2分子 | |
| D. | 2.8 g乙烯和丁烯的混合气体中所含原子数为0.2NA |
18.下列说法正确的是( )
| A. | H2的摩尔质量是2 g | B. | 1 mol H2O的质量是18 g/mol | ||
| C. | 氧气的摩尔质量是32 g/mol | D. | 2 g H2含1 mol H |