题目内容
7.某实验小组以粗镍(含少量Fe和Cr杂质)为原料制备Ni(NH3)6Cl2,并测定相关组分的含量.制备流程示意图如图.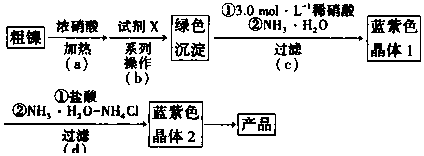
已知:①部分离子生成氢氧化物沉淀的pH(开始沉淀的pH按离子浓度为0.1mol•L-1计算)如表所示.
| Fe3+ | Cr3+ | Ni2+ | |
| 开始沉淀pH | 1.5 | 4.3 | 6.9 |
| 完全沉淀pH | 2.8 | 5.6 | 8.9 |
回答下列问题:
(1)实验需要配制3.0mol•L-1稀硝酸250mL.需要的玻璃仪器有烧杯、量筒、玻璃棒,胶头滴管和250mL容量瓶.
(2)步骤(a)中Ni和浓硝酸反应的化学方程式为Ni+4(浓)HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Ni(NO3)2+2NO2↑+2H2O.
(3)步骤(b)首先加入试剂x调节溶液的pH约为6,过滤后再继续加入X调节pH以得到绿色沉淀.
①调节pH约为6的原因是使Cr3+、Fe3+完全沉淀,而Ni2+未开始沉淀
②试剂X可以是C(填标号).
A.H2SO4 B.Ni(OH)2 C.NaOH D.Fe2O3 E.NiO
(4)步骤(c)和(d)中的反应都需要在冰水浴环境下进行,其作用除了可以减少氨水的挥发.还有降低温度以降低产物的溶解度而析出
(5)NH3含量的测定.[已知:Ni(NH3)6Cl2+6HCl=NiCl2+6NH4Cl]
i.用电子天平称量mg产品于锥形瓶中,用25mL水溶解后加入5mL的6mol•L-1盐酸,以甲基橙作指示剂,滴定至终点消耗0.500 0mol•L-1 NaOH标准溶液V1mL.
ii.空白试验:不加入样品重复实验i.消耗NaOH标准溶液V2 mL.
①NH3的质量分数为$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×8.5}{m}$×100%.
②在上述方案的基础上,下列措施中能进一步提高测定准确度的有AD(填标号).
A.适当提高称量产品的质量 B.用H2SO4溶液替代盐酸C.用酚酞替代甲基橙 D.进行平行试验.
分析 由实验流程及物质的性质可知,浓硝酸加热后离子主要有Ni2+、Cr3+、Fe3+,再加入试剂x调节溶液的pH约为6,使Cr3+、Fe3+完全沉淀,而Ni2+未开始沉淀,过滤后再继续加入X调节pH以得到绿色沉淀即Ni(OH)2,在加入稀硝酸、氨水,冰水浴结晶,过滤得到Ni(NH3)6(NO3)2的蓝紫色晶体1,再加入盐酸、氨水和氯化铵的混合溶液,再冰水浴结晶,过滤得到Ni(NH3)6Cl2的蓝紫色晶体2,最终得到产品,据此分析;
(1)根据配制一定物质的量浓度溶液用到仪器所需要的最主要仪器来选择;
(2)Ni和浓硝酸在加热条件下反应生成Ni(NO3)2、NO2和H2O;
(3)①根据以上分析,加入试剂x调节溶液的pH约为6主要是除去铁、铬杂质;
②根据试剂x的作用调节pH值到8.9得到绿色沉淀分析;
(4)根据冰水浴环境下即降低温度以降低产物的溶解度而析出分析;
(5)①根据滴定终点结合Ni(NH3)6Cl2+6HCl=NiCl2+6NH4Cl计算NH3的质量分数;
②适当提高称量产品的质量,数据过大能进一步提高测定准确度,进行平行试验取平均值能进一步提高测定准确度.
解答 解:(1)实验需要配制3.0mol•L-1稀硝酸250mL.需要的玻璃仪器除了有烧杯、量筒、玻璃棒,胶头滴管,还有250mL容量瓶,故答案为:250mL容量瓶;
(2)Ni和浓硝酸在加热条件下反应生成Ni(NO3)2、NO2和H2O,化学方程式为,Ni+4(浓)HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Ni(NO3)2+2NO2↑+2H2O,
故答案为:Ni+4(浓)HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Ni(NO3)2+2NO2↑+2H2O;
(3)①根据以上分析,加入试剂x调节溶液的pH约为6主要是使Cr3+、Fe3+完全沉淀,而Ni2+未开始沉淀,故答案为:使Cr3+、Fe3+完全沉淀,而Ni2+未开始沉淀;
②试剂x的作用是先调节pH约为6,后又要调节pH以得到绿色沉淀即要调到8.9,所以只有NaOH符合,故选:C;
故答案为:检验SO42-的操作为:取少量溶液Z于试管中,然后加盐酸,无沉淀产生,再加氯化钡溶液,有白色沉淀产生,证明有SO42-;
(4)冰水浴环境下其作用除了可以减少氨水的挥发,还有可以降低温度以降低产物的溶解度而析出,故答案为:降低温度以降低产物的溶解度而析出;
(5)①根据滴定,则不加入样品比加入mg产品多消耗氢氧化钠为(V2-V1)×10-3×0.500mol,所以mg产品NH3的物质的量为(V2-V1)×10-3×0.500mol,则NH3的质量分数为$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×0.500mol×17g/mol}{mg}$×100%=$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×8.5}{m}$×100%,故答案为:$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×8.5}{m}$×100%;
②适当提高称量产品的质量,数据过大能进一步提高测定准确度,进行平行试验取平均值能进一步提高测定准确度,而用H2SO4溶液替代盐酸、用酚酞替代甲基橙对实验基本没影响,故选:AD.
点评 本题主要考查了物质的制备及其相关组分的含量的测定等知识,较为综合,掌握实验方案的设计原理是解答的关键,题目难度中等.

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案下列说法中错误的是( )
| A. | KClO3在反应中得到电子 | |
| B. | ClO2中氯的化合价为+4价 | |
| C. | 在反应中H2C2O4是还原剂 | |
| D. | 1 mol KClO3参加反应有2mol电子转移 |
 人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )| A. | A为电源的负极 | |
| B. | 电解结束后,阴极室溶液的pH与电解前相比将不变 | |
| C. | 阳极室中发生的电极反应为2H++2e-═H2↑ | |
| D. | 若两极共收集到气体13.44 L(标准状况),则除去的尿素为18g(忽略气体的溶解) |
| A. | Ksp(CaF2)随温度和浓度的变化而变化 | |
| B. | 向1 L0.2 mol•L-1 HF溶液中加入1 L 0.2 mol•L-1 CaCl2溶液,没有沉淀产生 | |
| C. | AgCl不溶于水,不能转化为AgI | |
| D. | 常温AgCl若在NaI溶液中开始转化为AgI,NaI浓度必须不低于$\frac{1}{\sqrt{1.8}}$×10-11 mol•L-1 |
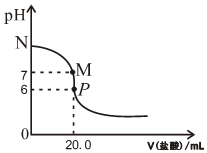 298K时,在20.0mL0.20mol•L-1氨水中滴入0.20mol•L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示.
298K时,在20.0mL0.20mol•L-1氨水中滴入0.20mol•L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示.