题目内容
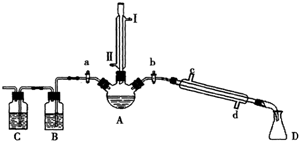
某兴趣小组同学在实验室用加热1-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,并检验反应的部分副产物,设计了如图所示装置,其中夹持仪器、加热仪器及冷却水管没有画出.
请根据实验步骤,回答下列问题:
(1)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷.竖直冷凝管接通冷凝水,进水口是 (填“I”或“Ⅱ”);冷凝回流的主要目的是 .
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等.熄灭酒精灯,在竖直冷凝管上方塞上塞子并打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物.B、C中应盛放的试剂分别是 和 ,写出C装置中主要的化学方程式: .
(3)为了进一步分离提纯1-溴丁烷,该兴趣小组同学查得相关有机物的数据如表所示:
请你补充下列实验步骤,直到分离出1-溴丁烷.
①待烧瓶冷却后,拔去竖直的冷凝管;
② ;③ ;④ ;⑤ ,收集所得馏分.
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g 1-溴丁烷,则1-溴丁烷的产率是 .(保留2位有效数字)

请根据实验步骤,回答下列问题:
(1)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷.竖直冷凝管接通冷凝水,进水口是
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等.熄灭酒精灯,在竖直冷凝管上方塞上塞子并打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物.B、C中应盛放的试剂分别是
(3)为了进一步分离提纯1-溴丁烷,该兴趣小组同学查得相关有机物的数据如表所示:
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
①待烧瓶冷却后,拔去竖直的冷凝管;
②
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g 1-溴丁烷,则1-溴丁烷的产率是
考点:制备实验方案的设计
专题:实验题
分析:(1)装置图分析冷凝回流的主要目的是提高反应物的利用率;
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等,能通过装置BC检出的是气体应检验1-丁烯、溴化氢的存在,先检验溴化氢的存在用石蕊试液或硝酸银溶液检验,后检验1-丁烯,选择试剂为溴水或高锰酸钾溶液褪色验证;C装置中主要的1-丁烯和溴单质发生加成反应;
(3)提纯1-溴丁烷,收集所得馏分为1-溴丁烷,所以须将1-溴丁烷先汽化,后液化,汽化须温度达其沸点101.6℃,需要理由蒸馏装置可知温度,冷却等操作规程设计步骤;
(4)依据化学方程式分析1-丁醇、NaBr反应情况,依据化学方程式计算生成的1-溴丁烷质量,依据产率=
×100%计算得到.
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等,能通过装置BC检出的是气体应检验1-丁烯、溴化氢的存在,先检验溴化氢的存在用石蕊试液或硝酸银溶液检验,后检验1-丁烯,选择试剂为溴水或高锰酸钾溶液褪色验证;C装置中主要的1-丁烯和溴单质发生加成反应;
(3)提纯1-溴丁烷,收集所得馏分为1-溴丁烷,所以须将1-溴丁烷先汽化,后液化,汽化须温度达其沸点101.6℃,需要理由蒸馏装置可知温度,冷却等操作规程设计步骤;
(4)依据化学方程式分析1-丁醇、NaBr反应情况,依据化学方程式计算生成的1-溴丁烷质量,依据产率=
| 实际量 |
| 理论量 |
解答:
解:(1)关闭a和b、接通竖直冷凝管的冷凝水,进水口为Ⅱ;给A加热30分钟,制备1-溴丁烷.冷凝回流的主要目的是,充分利用反应物,提高反应物的转化率,
故答案为:Ⅱ;充分反应,提高反应物的转化率;
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等,能通过装置B、C装置检出的是气体,应检验1-丁烯、溴化氢的存在,先检验溴化氢的存在用石蕊试液或硝酸银溶液检验,通过石蕊试液溶液变红色(通过硝酸银溶液生成浅黄色沉淀)证明溴化氢的生成;后检验1-丁烯,选择试剂为溴水或高锰酸钾溶液,通过为溴水或高锰酸钾溶液褪色证明生成的产物中含有1-丁烯,C装置中主要的化学方程式CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 ;
故答案为:石蕊试液(或AgNO3溶液);溴水(或酸性KMnO4溶液);CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 ;
(3)提纯1-溴丁烷,收集所得馏分为1-溴丁烷,所以须将1-溴丁烷先汽化,后液化,汽化须温度达其沸点101.6℃,利用蒸馏原理和装置设计的步骤为:
①待烧瓶冷却后,拔去竖直的冷凝管,②插上带橡皮塞的温度计 ③关闭a,打开b ④接通冷凝管的冷凝水,使冷水从d处流入 ⑤迅速升高温度至101.6℃;通过蒸到分离、提纯1-溴丁烷;
故答案为:插上带橡皮塞的温度计;关闭a,打开b;接通冷凝管的冷凝水,使冷水从d处流入;迅速升高温度至101.6℃;
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,依据化学方程式计算判断反应情况:
CH3CH2CH2CH2OH+NaBr+H2SO4
CH3CH2CH2CH2Br+NaHSO4+H2O
74 103
7.4g 10.3g
溴化钠过量,则1-丁醇全部反应生成1-溴丁烷物质的量为0.1mol,质量=0.1mol×137g/mol=13.7g;
蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g 1-溴丁烷,产率=
×100%=70%,
故答案为:70%.
故答案为:Ⅱ;充分反应,提高反应物的转化率;
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等,能通过装置B、C装置检出的是气体,应检验1-丁烯、溴化氢的存在,先检验溴化氢的存在用石蕊试液或硝酸银溶液检验,通过石蕊试液溶液变红色(通过硝酸银溶液生成浅黄色沉淀)证明溴化氢的生成;后检验1-丁烯,选择试剂为溴水或高锰酸钾溶液,通过为溴水或高锰酸钾溶液褪色证明生成的产物中含有1-丁烯,C装置中主要的化学方程式CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 ;
故答案为:石蕊试液(或AgNO3溶液);溴水(或酸性KMnO4溶液);CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 ;
(3)提纯1-溴丁烷,收集所得馏分为1-溴丁烷,所以须将1-溴丁烷先汽化,后液化,汽化须温度达其沸点101.6℃,利用蒸馏原理和装置设计的步骤为:
①待烧瓶冷却后,拔去竖直的冷凝管,②插上带橡皮塞的温度计 ③关闭a,打开b ④接通冷凝管的冷凝水,使冷水从d处流入 ⑤迅速升高温度至101.6℃;通过蒸到分离、提纯1-溴丁烷;
故答案为:插上带橡皮塞的温度计;关闭a,打开b;接通冷凝管的冷凝水,使冷水从d处流入;迅速升高温度至101.6℃;
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,依据化学方程式计算判断反应情况:
CH3CH2CH2CH2OH+NaBr+H2SO4
| △ |
74 103
7.4g 10.3g
溴化钠过量,则1-丁醇全部反应生成1-溴丁烷物质的量为0.1mol,质量=0.1mol×137g/mol=13.7g;
蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g 1-溴丁烷,产率=
| 9.6g |
| 13.7g |
故答案为:70%.
点评:本题主要考查了1-溴丁烷的制取实验,混合物分离的实验操作步骤和过程分析判断,明确反应原理是解答的关键,题目难度中等.

练习册系列答案
相关题目
下列离子方程式中正确的是( )
| A、碳酸氢钙溶液中加入过量氢氧化钠Ca2-+2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B、氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe2++3H2O |
| C、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O═AlO2-+2NH4++2H2O |
| D、Na2S溶液呈碱性:S2-+H2O=HS-+OH- |
下列现象不能用盐类水解知识解释的是( )
| A、明矾能用于净水 |
| B、泡沫灭火器的原理 |
| C、铜绿的生成 |
| D、配置FeCl2溶液时加入少量的盐酸 |
下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( )
| A、正丁烷 | B、异丁烷 |
| C、新戊烷 | D、异戊烷 |
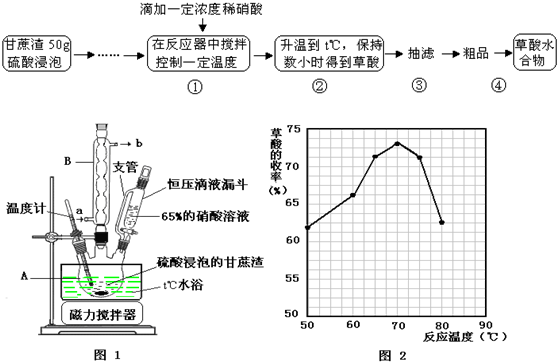
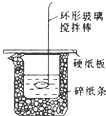 100mL0.55mol?L-1盐酸与100mL0.50mol?L-1氢氧化钠溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
100mL0.55mol?L-1盐酸与100mL0.50mol?L-1氢氧化钠溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题: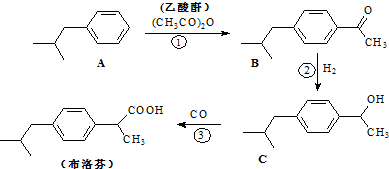

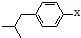 结构的酯类中共有6种(即X有不同的结构),请写出其中的二种
结构的酯类中共有6种(即X有不同的结构),请写出其中的二种