题目内容
20.(1)依据成键两原子间共用电子对是否有偏移,可将共价键分为极性键和非极性键.由此,请指出乙二醇分子中各共价键的类型极性键、非极性键.乙二醇的结构式为: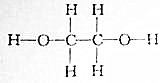
(2)依据成键两原子间共用电子的对数可将共价键分为单键、双键和三键.由此请指出丙烯腈分子中各共价键的类型单键、双键、三键.丙烯腈的结构式为
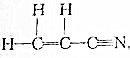
分析 (1)根据成键两原子间共用电子对是否有偏移,可将共价键分为极性键和非极性键;同种元素原子之间形成非极性键,不同元素原子之间形成极性键;
(2)依据成键两原子间共用电子的对数可将共价键分为单键、双键、三键.
解答 解:(1)成键两原子间共用电子对发生偏移为极性键,成键两原子间共用电子对不发生偏移为非极性键,乙二醇中碳与氧、碳与氢之间形成极性键,碳与碳之间形成非极性键,
故答案为:极性键、非极性键;极性键、非极性键;
是否有偏移,可将共价键分为极性键和非极性键;同种元素原子之间形成非极性键,不同元素原子之间形成极性键;
(2)依据成键两原子间共用电子的对数可将共价键分为单键、双键、三键,丙烯腈分子中含有碳氢单键、碳碳单键、碳碳双键、碳氮三键,
故答案为:单键、双键、三键;单键、双键、三键.
点评 本题考查共价键分类,注意从共用电子对偏移、共用电子对数、电子云重叠理解共价键类型,注意理解共价键极性与分子极性.

练习册系列答案
相关题目
10.“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是( )
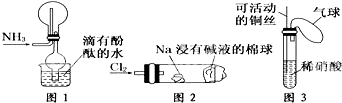
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中采用图3所示装置进行铜与稀硝酸的反应
④实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验.

①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中采用图3所示装置进行铜与稀硝酸的反应
④实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验.
| A. | ②③④ | B. | ①②④ | C. | ①②③ | D. | ①③④ |
11.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 1-己醇的沸点比己烷的沸点高89℃ | 1-己醇和己烷可通过蒸馏初步分离 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | H2SO4是离子化合物 | 硫酸溶液可导电 |
| D | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
| A. | A | B. | B | C. | C | D. | D |
5.下列物质属于碱的是( )
| A. | 苛性钠 | B. | 生石灰 | C. | 纯碱 | D. | 胆矾 |
12.氯气是一种化学性质很活泼的非金属单质,下列叙述中不正确的是( )
| A. | 能使潮湿的有色布条褪色 | |
| B. | 钠在氯气中燃烧,生成白色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
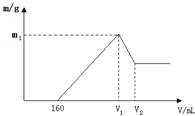 将镁铝的混合物0.1mol溶于100mL2mol/L硫酸溶液中,然后再滴加1mol/L氢氧化钠溶液,请回答以下问题:
将镁铝的混合物0.1mol溶于100mL2mol/L硫酸溶液中,然后再滴加1mol/L氢氧化钠溶液,请回答以下问题: