题目内容
8.焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈.发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X.(1)根据题意,可判断出X是H2O(写化学式).
(2)写出并配平该反应的化学方程式:6NH4Cl+4Fe2O3=6Fe+2FeCl3+3N2↑+12H2O;
(3)发生还原反应的物质是Fe2O3,反应中2mol的氧化剂能得到(填“失去”或“得到”)12mol电子.
(4)反应中被氧化产生了5.6L(标准状况)的气体时,被还原的物质的质量为40g.
分析 NH4Cl、FeCl3、N2、Fe2O3、Fe和X中,-3价N易失去电子,则氯化铵为还原剂,Fe得到电子,结合电子、原子守恒来解答.
解答 解:(1)由元素守恒可知,X中含H、O元素,X为H2O,故答案为:H2O;
(2)N元素的化合价由-3价升高为0,Fe元素的化合价由+3价降低为0,由电子、原子守恒可知反应为6NH4Cl+4Fe2O3=6Fe+2FeCl3+3N2↑+12H2O,
故答案为:6NH4Cl+4Fe2O3=6Fe+2FeCl3+3N2↑+12H2O;
(3)Fe元素的化合价降低,得到电子被还原,Fe2O3发生还原反应,由反应可知4mol氧化剂反应时转移24mol电子,则2mol氧化剂得到12mol电子,
故答案为:Fe2O3;得到;12;
(4)n(N2)=$\frac{5.6L}{22.4L/mol}$=0.25mol,由电子守恒可知被还原的物质的质量为$\frac{0.25mol×2×(3-0)}{2×(3-0)}$×160g/mol=40g,故答案为:40g.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化、电子守恒为解答的关键,侧重分析与应用能力的考查,注意电子守恒的应用,题目难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| B. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物有关 | |
| C. | 塑化剂是一种化工塑料软化剂,可以大量添加到婴幼儿玩具中 | |
| D. | 酒精可使蛋白质变性,故能消毒杀菌 |
19.向含MgCl2、AlCl3均为nmol的混合液中逐滴加入NaOH溶液至过量,生成沉淀与加入NaOH的物质的量关系正确的是( )(有关离子沉淀或沉淀溶解与pH关系如表)
| 离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
| 开始沉淀时的pH | 8.93 | 3.56 | 开始溶解时的pH | 8.04 |
| 完全沉淀时的pH | 10.92 | 4.89 | 完全溶解时的pH | 12.04 |
| A. | 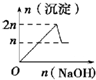 | B. |  | C. |  | D. | 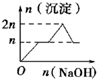 |
16.下列说法不正确的是( )
| A. | 天然气的主要成分是甲烷,它属于不可再生能源 | |
| B. | 煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料 | |
| C. | 石油分馏得到的汽油、煤油、柴油等都有混合物,没有固定的熔沸点 | |
| D. | 石油炼制的目的是为了获得轻质油和重要化工原料(乙烯、丙烯等) |
3.理论上下列反应不能设计成原电池反应的是( )
| A. | 2Fe3++Cu═2Fe2++Cu2+ | B. | Zn+2H+═Zn2++H2↑ | ||
| C. | 2H2+O2═2H2O | D. | H++OH-═H2O |
13.下列关于乙醇性质的化学方程式正确的是( )
| A. | 与金属钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |
| B. | 与氧气的燃烧反应:2CH3CH2OH+O2$\stackrel{点燃}{→}$2CH3CHO+2H2O | |
| C. | 与氧气的催化氧化:CH3CH2OH+3O2$→_{△}^{Cu或Ag}$2CO2+3H2O | |
| D. | 与乙酸的酯化反应:CH3CH2OH+CH3COOH$→_{△}^{催化剂}$CH3CH2OCH2CH3 |
17.在温度不变的条件下,恒定的容器中进行下列反应:N2O4?2NO2,若N2O4的浓度由0.1mol/L降到0.07mol/L要用10s,那么N2O4的浓度从0.07mol/L降到0.04mol/L时,所用时间( )
| A. | 等于10s | B. | 等于5 s | C. | 大于10 s | D. | 小于10 s |