题目内容
4.某固体混合物可能由KCl、K2SO4、CuCl2、CaCl2、K2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验:(1)混合物中加入足量水得一无色透明溶液;
(2)上述溶液中滴加BaCl2有白色沉淀产生;
(3)过滤,然后向上述白色沉淀加盐酸时,沉淀全部溶解;
(4)往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸.
试判断:
①肯定存在的物质有K2CO3;
②肯定不存在的物质有K2SO4、CuCl2、CaCl2;
③可能存在的物质有KCl.
④写出下列实验步骤中发生反应的离子方程式:
步骤(3)BaCO3+2H+=Ba2++H2O+CO2↑
步骤(4)Cl-+Ag+=AgCl↓.
分析 混合物中加入足量水得一无色透明溶液,说明不含CuCl2,滴加BaCl2有白色沉淀产生,加盐酸时,沉淀全部溶解,说明生成的沉淀为BaCO3,则混合物中含有K2CO3,不含K2SO4,混合物中含有K2CO3,则一定不含有CaCl2,往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸,该沉淀为AgCl,但因(3)操作中加入盐酸不能确定是否含有KCl.
解答 解:(1)混合物中加入足量水得一无色透明溶液,说明不含CuCl2,
(2)滴加BaCl2有白色沉淀产生,可能为BaCO3或BaSO4,
(3)加盐酸时,沉淀全部溶解,说明生成的沉淀为BaCO3,则混合物中含有K2CO3,不含K2SO4,混合物中含有K2CO3,则一定不含有CaCl2,
(4)往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸,该沉淀为AgCl,但因(3)操作中加入盐酸不能确定是否含有KCl,另外NaNO3不与其它物质反应,也不能确定,所以,肯定存在的物质有K2CO3,肯定不存在的物质有K2SO4、CuCl2、CaCl2,可能存在的物质有KCl.
①肯定存在的物质有K2CO3,故答案为:K2CO3;
②肯定不存在的物质有K2SO4、CuCl2、CaCl2;故答案为:K2SO4、CuCl2、CaCl2;
③可能存在的物质有KCl.
故答案为:KCl.
④加盐酸时,沉淀全部溶解,说明生成的沉淀BaCO3完全溶于盐酸中,即BaCO3+2H+=Ba2++H2O+CO2↑;往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸,次沉淀是氯化银沉淀,证明含有氯离子,发生反应为:Cl-+Ag+=AgCl↓.故答案为:BaCO3+2H+=Ba2++H2O+CO2↑;Cl-+Ag+=AgCl↓.
点评 本题考查未知物的经验,题目难度不大,本题注意根据物质反应的现象进行推断,学习中注重常见元素化合物知识的积累.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 同位素:1H、D+、T2 | |
| B. | 电解质:CaCO3、CH3COOH、NH4HCO3 | |
| C. | 胶体:饱和氯化铁溶液、淀粉溶液、牛奶 | |
| D. | 硅酸盐产品:晶体硅、水泥、陶瓷 |
| A. | 纤维素 涤纶 | B. | 麦芽糖 胰岛素 | ||
| C. | 聚乙烯 酚醛树脂 | D. | 淀粉 聚异戊二烯 |
| 物质 | 杂质 | 除杂试剂或方法 |
| (1)FeCl3溶液 | FeCl2 | |
| (2)FeCl2溶液 | FeCl3 | |
| (3)FeSO4溶液 | CuSO4 | |
| (4)Na2CO3 | NaHCO3 | |
| (5)Mg (OH)2 | Al(OH)3 | , |
| A. | 向某溶液中加入稀硝酸酸化,再滴入BaCl2溶液,产生白色沉淀,则原溶液中一定有SO42- | |
| B. | 向某溶液中加入稀硫酸酸化,再滴入AgNO3溶液,产生白色沉淀,则原溶液中一定有Cl- | |
| C. | 向某溶液中加入碳酸钠溶液,产生白色沉淀,再滴入稀盐酸,沉淀溶解,则原溶液中一定有Ca2+ | |
| D. | 用光洁的铂丝蘸取某无色溶液,在酒精灯外焰里灼烧时观察到黄色火焰,则原溶液中一定有Na+ |
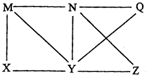 现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )| A. | X可能为Al或Cl2 | B. | Y一定为NaOH(aq) | ||
| C. | N一定是HCl(aq) | D. | Q、Z中的一种必定为Al2O3 |
| A. | FeCl3 | B. | Cu(NO3)2 | C. | Na2SO3 | D. | Al2(SO4)3 |