题目内容
3.设NA为阿伏伽德罗常数的值,下列叙述中不正确的是( )| A. | 0.1molNaCl固体中含0.1NA个阳离子 | |
| B. | 22.4LCO2含有的原子数是3NA | |
| C. | 常温常压下,NA个H2质量为2g | |
| D. | 1molMg与足量O2反应,失去的电子数是2NA |
分析 A.1mol氯化钠中含有1mol钠离子和1mol氯离子;
B.气体状况未知;
C.依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$计算解答;
D.镁与氧气反应生成氧化镁,氧化镁中镁为+2价.
解答 解:A.0.1molNaCl固体中含0.1mol钠离子,即含有0.1NA个阳离子,故A正确;
B.气体状况未知,Vm不确定,无法计算二氧化碳物质的量和所含原子个数,故B错误;
C.常温常压下,NA个H2物质的量为1mol,质量为:1mol×2g/mol=2g,故C正确;
D.1molMg与足量O2反应生成1mol氧化镁,失去的电子数是2NA,故D正确;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大,注意气体摩尔体积使用条件和对象.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
9.下列反应的离子方程式书写正确的是( )
| A. | 氯化铁溶液与铜反应:Fe3++Cu═Fe2++Cu2+ | |
| B. | 氢氧化铁与稀盐酸反应:OH-+H+═H2O | |
| C. | 钠与水的反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
14.短周期元素a、b、c、d原子序数依次增大,a的核外电子总数与其周期数相同,b的某种单质是空气的主要成分,c的最外层电子数为其内层电子数的3倍,d与c同族:下列说法错误的是( )
| A. | a、b、d均可以与c形成两种或多种二元化合物 | |
| B. | d的原子半径是这些元素中最大的 | |
| C. | a与d形成的化合物可以抑制水的电离 | |
| D. | 常温下,由这四种元素构成的某种盐的溶液pH=4,则水电离出的H+浓度肯定是1×10-4mol/L |
11.下列说法不正确的是( )
| A. | 乙酸和甲醛分别完全燃烧,若消耗的氧气量一样,则它们的质量相等 | |
| B. | 铜丝表面的黑色氧化膜可用酒精除去 | |
| C. | Na2CO3溶液可使苯酚浊液变澄清 | |
| D. | 含0.01mol甲醛的福尔马林溶液与足量的银氨溶液充分反应,生成2.16gAg |
18.下列关于${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl说法正确的是( )
| A. | 具有相同的质子数 | B. | 具有相同的中子数 | ||
| C. | 具有相同的质量数 | D. | 它们不互为同位素 |
8.亚硝酸钠(NaNO2)俗称“工业盐”,其外观与食盐相似,有咸味,有毒,可用做食品防腐剂和肉类食品的发色剂.已知亚硝酸钠能与氢碘酸(HI,具有强酸性)发生如下反应:4HI+2NaNO2═2NaI+I2+2NO↑+2H2O.下列说法正确的是( )
| A. | 亚硝酸钠具有氧化性,不可能表现出还原性 | |
| B. | 该反应中氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 向反应所得的混合溶液中加入稀硫酸和亚硝酸钠,I-不可能转化为I2 | |
| D. | 人误食亚硝酸钠中毒时,可服用氢碘酸解毒 |
15.下列有关实验的说法正确的是( )
| A. | 用pH试纸测双氧水的pH | |
| B. | 用酸式滴定管量取20.00 mL酸性KMnO4溶液 | |
| C. | 用托盘天平称取 5.85 g NaCl晶体 | |
| D. | 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液 |
12.利用下列装置不能完成对应实验的是( )
| A. |  实验室制取氨气 | B. | 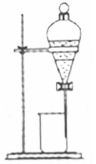 用CCl4萃取碘水中的碘 | ||
| C. | 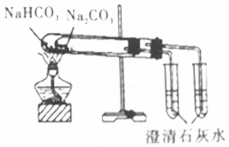 比较Na2CO3与NaHCO3的稳定性 | D. | 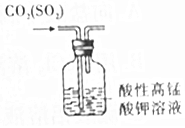 除去CO2中混有的少量SO2 |
8.下列物质中,既能溶于强酸溶液又能溶于强碱溶液的氧化物是( )
| A. | MgO | B. | Al2O3 | C. | SiO2 | D. | Al(OH)3 |