题目内容
3.卤代烃的制备有多种方法,下列卤代烃不能由相应的烃经加成反应制得的是( )| A. | 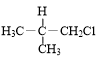 | B. | 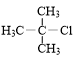 | C. | 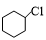 | D. | 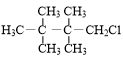 |
分析 如果卤代烃中连接卤原子的碳原子相邻碳原子上含有H或卤原子,则该卤代烃可以由烃经过加成反应制得,据此分析解答.
解答 解:A.该卤代烃连接氯原子的碳原子相邻碳原子上含有H原子,所以该卤代烃可以由2-甲基丙烯和HCl发生加成反应得到,故A不选;
B.该卤代烃连接氯原子的碳原子相邻碳原子上含有H原子,该氯代烃由2-甲基丙烯和HCl发生加成反应得到,故B不选;
C.该氯代烃中连接氯原子的碳原子上相邻碳原子上含有H原子,该氯代烃可以有环己烯和HCl发生加成反应得到,故C不选;
D.该氯代烃中连接氯原子的碳原子相邻碳原子上没有H原子,所以不能有烃发生加成反应得到,故D选;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确有机物官能团及其性质关系是解本题关键,采用逆向思维方法分析解答,也可以根据该氯代烃发生消去反应判断,题目难度不大.

练习册系列答案
相关题目
13.a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
其中:b的离子半径大于e的离子半径;d是溶于显碱性的四原子分子;g是常见的一种液体.试写出:
(1)a微粒的结构示意图是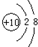 .
.
(2)b与e相应元素的最高价氧化物的水化物的碱性强弱比较为:NaOH>Mg(OH)2(用化学式表示).
(3)d的水溶液显碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.
(4)c微粒的电子式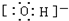 .
.
(5)b相应的元素的单质与g微粒反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
| 微粒代码 | a | b | c | d | e | f | g |
| 原子核数目 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 带电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)a微粒的结构示意图是
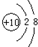 .
.(2)b与e相应元素的最高价氧化物的水化物的碱性强弱比较为:NaOH>Mg(OH)2(用化学式表示).
(3)d的水溶液显碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.
(4)c微粒的电子式
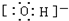 .
.(5)b相应的元素的单质与g微粒反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
14.已知X、Y、Z均为短周期元素,它们之间可形成X2Z和YZ2两种化合物,X、Y、Z的原子序数依次增大,X原子K层的电子数只有一个,Y位于X的下一周期,它的最外层电子数比K层多2个,而Z原子核外的最外层电子数比次外层少2个,请回答下列问题;
(1)它们的元素符号分别为:XH,YC,ZS.
(2)用价层电子对互斥理论判断:
(3)N2O双称笑气,N2O与YZ2具有相似的分子结构,请分析原因:二者互为等电子体.
(1)它们的元素符号分别为:XH,YC,ZS.
(2)用价层电子对互斥理论判断:
| 物质 | 分子的价层电子对数 | 中心原子的杂化轨道类型 | 分子的立体构型名称 |
| X2Z | V形 | ||
| YZ2 |
11.有四种试剂:①AgNO3 ②HNO3 ③新制Cu(OH)2 ④碘水.为依次鉴别葡萄糖溶液、淀粉溶液、食盐溶液、鸡蛋清溶液,加入上述试剂的正确顺序是( )
| A. | ④②①③ | B. | ①③②④ | C. | ③②④① | D. | ③④①② |
8.下列有关实验现象或叙述中,不正确的是( )
| A. | 氢气在Cl2中燃烧,发出苍白色火焰 | |
| B. | 铵盐与碱共热产生气体能使干燥的红色石蕊试纸变蓝 | |
| C. | 实验室制氯气用饱和食盐水除去氯化氢 | |
| D. | 铜丝在Cl2中燃烧,生成棕黄色烟 |
15.下列关于有机物的叙述中正确的是( )


| A. | 油脂在稀硫酸或氢氧化钠溶液中均可发生水解反应,水解产物相同 | |
| B. | 取淀粉与稀硫酸共热后的溶液,加入新制银氨溶液共热,没有银镜产生,说明淀粉尚未水解生成葡萄糖 | |
| C. | 结构式为如上图所示的有机物,可以在稀硫酸催化下发生水解反应,但水解产物只有一种 | |
| D. | 纤维素、蔗糖、葡萄糖、蛋白质在一定条件下均可发生水解 |
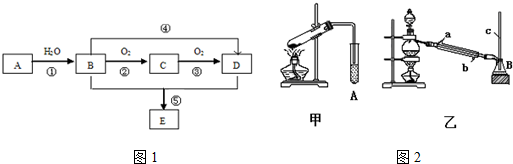
 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,E是重要的建筑材料,F可用于清除铁锈.它们之间的转化关系如图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题:
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,E是重要的建筑材料,F可用于清除铁锈.它们之间的转化关系如图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题: