题目内容
能源是影响全球经济和生活的重要因素.目前人类已开发和利用的能源中,氢气是最理想的清洁能源之一.已知反应:2H2+O2
2H2O,试回答下列问题.
(1)该反应为 反应(填“吸热”或“放热”);
(2)当生成18gH2O时,H2O的物质的量是 (填字母代号).
A.1mol B.1mol/L C.1g/mol.
| ||
(1)该反应为
(2)当生成18gH2O时,H2O的物质的量是
A.1mol B.1mol/L C.1g/mol.
考点:吸热反应和放热反应,物质的量的相关计算
专题:
分析:(1)根据反应类型判断得出正确结论;
(2)根据质量与物质的量的关系式得出正确结论.
(2)根据质量与物质的量的关系式得出正确结论.
解答:
解:(1)燃烧反应都是放热反应,故答案为:放热;
(2)n(H2O)=
=1mol,故答案为:A.
(2)n(H2O)=
| 18g |
| 18g/mol |
点评:本题考查物质的量的相关计算,物质的量的相关计算是高考不变的一个题型,每年高考必考,是热点题型,题目难度不大,同时注意燃烧反应都是放热反应.

练习册系列答案
相关题目
下列操作过程中使溶液导电性基本不变的是( )
| A、100ml自来水中加入0.01molNaOH固体 |
| B、100ml 0.5mol/L的NaOH中通入0.05mol氯气 |
| C、100ml0.5mol/L的醋酸中加入100ml 0.5mol/L的氨水 |
| D、100ml 0.1mol/L的氯水中通入0.01molSO2气体 |
将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是( )
| A、Ca(OH)2的溶解度、溶剂的质量 |
| B、溶液中溶质的质量分数 |
| C、溶液的质量、水的电离平衡 |
| D、溶液中Ca2+的数目、溶液中Ca2+的浓度 |
下列现象的产生与人为排放大气污染物氮氧化物无关的是( )
| A、闪电 | B、光化学烟雾 |
| C、酸雨 | D、臭氧层空洞 |
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
| A、电子数之比1:1 |
| B、体积比16:11 |
| C、密度比16:11 |
| D、氧原子数之比为1:1 |
下列反应的离子方程式正确的是( )
| A、氢氧化钡中加入稀硫酸:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |
| B、氧化铜溶于稀硫酸:2H++CuO=Cu2++H2O |
| C、碳酸钙溶于盐酸:CO32-+2H+=CO2↑+H2O |
| D、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ |
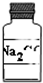 固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )
固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )| A、只用盐酸一种试剂就可以确定该固体A的成分 |
| B、依次加入Ba(NO3)2溶液、盐酸,若有白色沉淀,则固体A为Na2SO4 |
| C、滴入酸性KMnO4溶液,若KMnO4溶液褪色,则固体A为Na2SO3 |
| D、用pH试纸检验(常温),若pH>7,则固体A可能是Na2CO3 |