题目内容
8.下列实验装置,试剂选用或操作正确的是( )| A. | 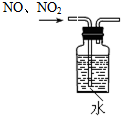 除去NO中的NO2 | B. | 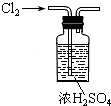 干燥Cl2 | C. | 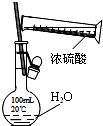 稀释浓硫酸 | D. |  制备少量O2 |
分析 A.二氧化氮与水反应生成NO,但装置内部有空气;
B.干燥时气体长进短出,浓硫酸与氯气不反应;
C.不能在容量瓶中稀释;
D.过氧化钠为粉末状固体,关闭活塞不能控制反应的停止.
解答 解:A.二氧化氮与水反应生成NO,但装置内部有空气,应将试剂瓶充满水,故A错误;
B.干燥时气体长进短出,浓硫酸与氯气不反应,浓硫酸具有吸水性,则该装置可干燥氯气,故B正确;
C.不能在容量瓶中稀释,应在烧杯中稀释、冷却后转移到容量瓶中,故C错误;
D.过氧化钠为粉末状固体,关闭活塞不能控制反应的停止,则该装置不能制备少量氧气,故D错误;
故选B.
点评 本题考查化学实验方案的评价及实验装置综合应用,为高频考点,把握物质的性质、实验技能、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.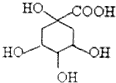 奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中不正确的是( )
奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中不正确的是( )
 奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中不正确的是( )
奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中不正确的是( )| A. | 不能使溴的四氯化碳溶液褪色 | |
| B. | 能用碳酸氢钠溶液鉴别奎尼酸和苯 | |
| C. | 1 mol奎尼酸与足量钠反应生成56L氢气 | |
| D. | 与乙醇、乙酸均能发生取代反应 |
19.将7g某铜、银合金与足量的a mol/L HNO3充分反应,完全溶解后放出的气体与标准状况下的氧气0.56L混合,通入水中恰好完全吸收,则此合金中铜的质量是( )
| A. | 1.6 g | B. | 2.4 g | C. | 3.2 g | D. | 4.8 g |
3.某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+、K+等8种离子中的某几种.取该溶液进行实验,得到如下现象:( )
①向溶液中滴加过量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断:该溶液中存在的离子组可能是.
①向溶液中滴加过量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断:该溶液中存在的离子组可能是.
| A. | Al3+、Mg2+、SO32- | B. | K+、CO32-、I- | C. | Al3+、CO32-、I- | D. | Na+、Br-、CO32- |
13.化学与生产、生活密切相关.下列叙述不正确的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 葡萄糖注射液不能产生丁达尔效应,不属于胶体 | |
| C. | 蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生无关 |
17.I:工业制硫酸时,利用接触氧化反应将SO 2转化为SO3是一个关键步骤.
(1)某温度下,2SO2(g)+O2(g)═2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0 mol O2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(mol/L)-1(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件
(以V2O5作催化剂)温度450℃;压强1×105Pa,选择此压强的理由再增压转化率增大不明显,加大成本
(4)能判断该反应达到平衡状态的依据是ACF
A.容器的压强不变 B.混合气体的密度不变 C.混合气体中SO3的浓度不变
D.c(SO2)=c(SO3) E.v正(SO2)=v 正(SO3) F.v正(SO3)=2v逆(O2)
(1)某温度下,2SO2(g)+O2(g)═2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0 mol O2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(mol/L)-1(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件
(以V2O5作催化剂)温度450℃;压强1×105Pa,选择此压强的理由再增压转化率增大不明显,加大成本
| 1×l05 Pa | 5×l05 Pa | 10×l05 Pa | 50×l05 Pa | 100×l05 Pa | |
| 450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.容器的压强不变 B.混合气体的密度不变 C.混合气体中SO3的浓度不变
D.c(SO2)=c(SO3) E.v正(SO2)=v 正(SO3) F.v正(SO3)=2v逆(O2)
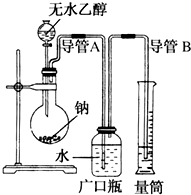 为了确定乙醇分子的结构简式是CH3-O-CH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子数目.试回答下列问题:
为了确定乙醇分子的结构简式是CH3-O-CH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子数目.试回答下列问题: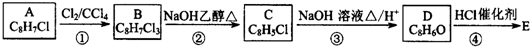
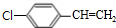 ,B中含有的官能团是氯原子.
,B中含有的官能团是氯原子.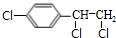 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$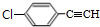 +2NaCl+2H2O,其反应类型为消去反应.
+2NaCl+2H2O,其反应类型为消去反应.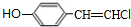 ;
;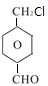 、
、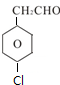 .
.