题目内容
3.某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+、K+等8种离子中的某几种.取该溶液进行实验,得到如下现象:( )①向溶液中滴加过量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断:该溶液中存在的离子组可能是.
| A. | Al3+、Mg2+、SO32- | B. | K+、CO32-、I- | C. | Al3+、CO32-、I- | D. | Na+、Br-、CO32- |
分析 ①向溶液中滴加足量氯水后,溶液变橙色,说明溶液中含有Br-,且有无色气泡冒出,说明溶液中含离子CO32-;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明不含SO32-;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色,可能是碘离子氧化成单质碘,进一步单质碘被氧化成碘酸根离子或溶液中不含I-,所以溶液不变色,不能确定碘离子存在,以此来解答.
解答 解:①向溶液中滴加足量氯水后,溶液变橙色,说明溶液中含有Br-,且有无色气泡冒出,说明溶液中含离子CO32-;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明不含SO32-;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色,可能是碘离子氧化成单质碘,进一步单质碘被氧化成碘酸根离子或溶液中不含I-,所以溶液不变色,不能确定碘离子存在;
溶液中含有CO32-,则一定不含有Al3+、Mg2+,因与CO32-反应生成沉淀,
根据溶液呈电中性原则,溶液中一定含有Na+或K+,
所以溶液中一定不存在的离子为Al3+、Mg2+、SO32-,
该溶液中存在的离子组可能是CO32-、Br-、Na+或K+、CO32-、I-,
故选BD.
点评 本题考查常见离子的检验,为高频考点,把握常见离子之间的反应、离子共存、溶液为电中性为解答的关键,侧重分析与推断能力的综合考查,充分考查了学生灵活应用基础知识的能力,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列有关叙述正确的是( )
| A. | 丁达尔现象是化学变化 | |
| B. | 钠能与硫酸铜稀溶液反应,置换出红色的铜 | |
| C. | 定容时,因不慎使液面高于容量瓶的刻度线,需重新配制 | |
| D. | 氢氧化铁胶体在直流电场中,一段时间阴极附近红褐色加深,说明胶体带正电 |
11.X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成Z2Y2、Z2Y、RY3、XW4等类型的化合物,其中Y、R同主族,Z、R、W同周期.下列说法正确的是( )
| A. | 各元素对应的离子半径顺序为:R>W>Z>Y | |
| B. | 气态氢化物的稳定性及还原性:HmW>HnR | |
| C. | XYR、X2W6、R2W2分子中所有原子均满足8电子结构 | |
| D. | 某气体通入品红溶液,溶液颜色褪去,则该气体一定是RY2 |
18.下列各项中表达正确的是( )
| A. | CO2分子的结构式:O=C=O | B. | NaCl的电子式: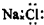 | ||
| C. | N2的结构式: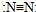 | D. | F的原子结构示意图: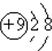 |
8.下列实验装置,试剂选用或操作正确的是( )
| A. | 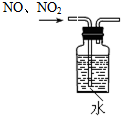 除去NO中的NO2 | B. | 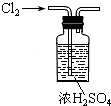 干燥Cl2 | C. | 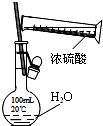 稀释浓硫酸 | D. |  制备少量O2 |
15.一定能在下列溶液中大量共存的离子组是( )
| A. | pH=0的溶液:Fe2+、Mg2+、NO3-、SO42- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- | |
| D. | pH=12的溶液:Na+、K+、〔Al(OH)4〕-、CO32- |
12.化学与社会可持续发展密切相关.下列做法不合理的是( )
| A. | CO2和氢气合成甲烷,实现“碳循环” | |
| B. | 提倡步行、骑自行车、乘公交车等“低碳”出行方式 | |
| C. | 采用纳米TiO2光触媒技术将装修材料中释放的HCHO转化为无害物质 | |
| D. | 将造纸废水通过高压水井压到地下或溶洞中,减少对地表水的污染 |