题目内容
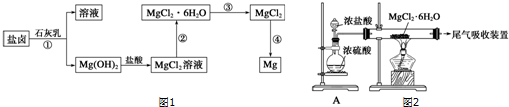
6.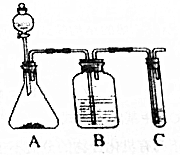 利用如图装置还可以验证醋酸、苯酚、碳酸的酸性强弱.
利用如图装置还可以验证醋酸、苯酚、碳酸的酸性强弱.(1)A中固体试剂是b(选填字母);
a.醋酸钠 b.碳酸氢钠 c.苯酚钠
(2)C中反应的化学方程式是:
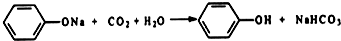 ;
;(3)有同学认为没有B装置,也可以验证酸性的强弱,这种认为是不合理的,原因是不合理,乙酸有挥发性且能和苯酚钠反应,干扰CO2与苯酚钠的反应(3)乙酸有挥发性且能和苯酚钠反应,干扰CO2与苯酚钠的反应.
分析 验证醋酸、苯酚、碳酸的酸性强弱,由实验装置可知,分液漏斗中为醋酸,锥形瓶中为碳酸氢钠,B中饱和碳酸氢钠溶液除去挥发的醋酸,C中为苯酚钠,发生强酸制取弱酸的反应,以此来解答.
解答 解:验证醋酸、苯酚、碳酸的酸性强弱,由实验装置可知,分液漏斗中为醋酸,锥形瓶中为碳酸氢钠,B中饱和碳酸氢钠溶液除去挥发的醋酸,C中为苯酚钠,发生强酸制取弱酸的反应,
(1)A中固体试剂是碳酸氢钠,故答案为:b;
(2)苯酚钠与碳酸反应生成苯酚和碳酸氢钠,化学反应方程式为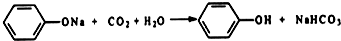 ,
,
故答案为: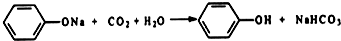 ;
;
(3)由于醋酸具有挥发性,若不除去挥发出来的醋酸,会对后续实验造成干扰,故答案为:不合理,乙酸有挥发性且能和苯酚钠反应,干扰CO2与苯酚钠的反应(3)乙酸有挥发性且能和苯酚钠反应,干扰CO2与苯酚钠的反应.
点评 本题考查性质实验设计及实验装置综合应用,为高频考点,把握强酸制取弱酸的反应原理及装置B的作用为解答的关键,侧重分析与实验能力的考查,注意醋酸易挥发,题目难度不大.

练习册系列答案
相关题目
16.常温下,某无色透明的溶液中,下列各组离子能够大量共存的是( )
| A. | H+、Na+、Cl-、HCO3- | B. | Ba2+、Na+、SO42-、Cl- | ||
| C. | MnO4-、K+、S2-、H+ | D. | Mg2+、Cl-、NO${\;}_{3}^{-}$、H+ |
1.下列各组排列顺序,正确的是( )
| A. | 微粒半径:K>Ca>H | B. | 碱性强弱:Mg(OH)2>Ca(OH)2>Ba(OH)2 | ||
| C. | 最高化合价:F>N>Si | D. | 热稳定性:HF>H2S>H2O |
11.芳香族化合物A的分子式为C9H10O2,A能与碳酸氢钠溶液反应产生气体,则A的结构(不考虑立体异构)最多有( )
| A. | 11种 | B. | 12种 | C. | 13种 | D. | 14种 |
18.若在加入铝粉能放出氢气的无色溶液中,分别加入下列各组离子,可能共存的是( )
| A. | NH4+、CO32-、K+、Na+ | B. | Na+、Ba2+、Cl-、HCO32- | ||
| C. | NO3-、Cu2+、K+、SO42- | D. | NO3-、K+、CO32-、OH- |
12.六种元素X、Y、Z、M、N、Q的原子序数依次增大且不大于18,其中X与N同主族,Y与Q同主族,N与Q同周期.已知常温下单质X与N的状态不同,M的核电荷数是Y的最外层电子数的2倍,单质Q是一种重要的半导体材料,下列推断中正确的是( )
| A. | 由X、Z、M三种元素组成的化合物一定是共价化合物 | |
| B. | Q与M形成的化合物可以作为光导纤维的主要原料,且不与任何酸反应 | |
| C. | 元素的非金属性由强到弱的顺序:M>Z>Q>Y | |
| D. | 原子半径由大到小的顺序:N>Q>Z>M |
13.下列物质中既能与盐酸反应,又能与氢氧化钠溶液反应( )
| A. | NaHCO3 | B. | NaHSO4 | C. | NH4Cl | D. | AlCl3 |