题目内容
19.水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )| A. | 氨水的电离程度 | B. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | C. | c(H+)和c(OH-)的乘积 | D. | OH-的物质的量 |
分析 氨水是弱碱,存在电离平衡,稀释促进电离,OH-的物质的量增加,但浓度减小,所以氢离子的浓度增加.NH3•H2O的物质的量减小,浓度减小,所以溶液中随着水量的增加而减小的是$\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$,以此解答该题.
解答 解:在氨水中存在如下电离平衡:NH3.H2O=NH4++OH-,
A.一水合氨存在电离平衡,加水稀释促进电离,氨水的电离程度增大,故A错误;
B.k=$\frac{c(N{{H}_{4}}^{+})c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$,用水稀释0.1mol/L氨水时,c(NH4+)变小,因温度不变,则K不变,所以有$\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$减小,故B正确;
C.由于温度不变,所以c(H+)和c(OH-)的乘积不变,故C错误;
D.稀释促进电离,OH-的物质的量增加,故D错误.
故选B.
点评 本题考查了电离常数,水的离子积,该考点是高考考查的重点,解题的关键是温度不变,水的离子积不变,电离常数也不变,题目难度中等.

练习册系列答案
相关题目
9.下列物质中既含有离子键又含有共价键的是( )
| A. | MgCl2 | B. | NaOH | C. | H2O2 | D. | H2SO4 |
10.有关晶体的结构如图所示,下列说法中不正确的是( )
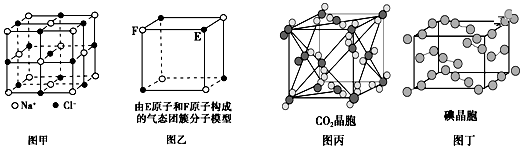

| A. | 在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体 | |
| B. | 该气态团簇分子(图乙)的分子式为EF或FE | |
| C. | 在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻 | |
| D. | 在碘晶体(图丁)中,存在非极性共价键和范德华力 |
7.化学与生活息息相关,下列说法不正确的是( )
| A. | 用食醋可除去热水壶内壁的水垢 | B. | 医用酒精的浓度通常为95% | ||
| C. | 烹鱼时加适量醋和酒可以增加香味 | D. | 碘盐中的碘不可以直接用淀粉检验 |
14.下列既有离子键又有共价键的化合物是( )
| A. | NaCl | B. | Na2O | C. | CaF2 | D. | Na2O2 |
4.对下列事故预防或处理方法正确的是( )
| A. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硫酸 | |
| B. | 欲配置500 mL l mol/LNaOH溶液,应将20gNaOH固体溶于500 mL水中 | |
| C. | 稀释浓硫酸时,为防止液体飞溅,将浓硫酸沿烧杯壁缓缓加入水中,并不断搅拌 | |
| D. | 钠着火时用二氧化碳灭火 |
11.在密闭的容器中的一定量混合气体发生反应,xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容器扩大到原来的两倍,在达平衡时,测得A的浓度降低为0.5mol/L.下列有关判断正确的是( )
| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | B的转化率升高 | D. | C的体积分数下降 |
8.下列物质中既有离子键又有共价键的是( )
| A. | KOH | B. | H2O | C. | CaCl2 | D. | Cl2 |
3. 常温下,将11.65g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
常温下,将11.65g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
( )
 常温下,将11.65g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
常温下,将11.65g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是( )
| A. | 相同温度时,Ksp(BaSO4)>Ksp(BaCO3) | |
| B. | BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 | |
| C. | 若使0.05molBaSO4全部转化为BaCO3,至少要加入1.25molNa2CO3 | |
| D. | 0.05molBaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(OH-)>c(Ba2+) |