题目内容
8.下列物质中既有离子键又有共价键的是( )| A. | KOH | B. | H2O | C. | CaCl2 | D. | Cl2 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.KOH含离子键、O-H共价键,故A选;
B.水只含共价键,故B不选;
C.氯化钙只含离子键,故C不选;
D.氯气只含共价键,故D不选;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键及特例,题目难度不大.

练习册系列答案
相关题目
18.下列物质晶体类型和化学键类型完全相同的是( )
| A. | MgCl2 NaOH | B. | HCl SiO2 | C. | NaOH NH4Cl | D. | 红磷 金刚石 |
19.水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
| A. | 氨水的电离程度 | B. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | C. | c(H+)和c(OH-)的乘积 | D. | OH-的物质的量 |
16.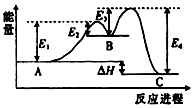 某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )
某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )
 某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )
某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )| A. | 两步反应均为吸热反应 | B. | 加入催化剂可以改变A→C的反应热 | ||
| C. | 三种化合物中C最稳定 | D. | 整个反应中△E=E4-E1-E2-E3 |
3.X(g)+3Y(g)?2Z(g)△H=-a kJ•mol-1,一定条件下,将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol.下列说法不正确的是( )
| A. | 10min内,Z的平均反应速率为0.02 mol•L-1•min-1 | |
| B. | 第10min时,X的物质的量浓度为0.8mol•L-1 | |
| C. | 10min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10min内,X和Y反应放出的热量为0.2a kJ |
13.已知一定温度下,2X(g)+Y(g) 2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )
2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )
 2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )
2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )| A. | 2b=c | B. | a=b | C. | a>2c | D. | 以上都不正确 |
20.以下所采取的分离方法正确的是( )
| A. | 由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来 | |
| B. | 由于胶体微粒的直径比离子大,所以碘化钾混入淀粉中可用渗析法分离 | |
| C. | 可用冷却热的饱和氯化钾和氯化钠混合溶液的方法得到纯净的氯化钠晶体 | |
| D. | 水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精 |
17.X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素.X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素.下列说法不正确的是( )
| Y | Z | M | |
| W |
| A. | 原子半径:W>Y>Z>M>X | |
| B. | N的一种氧化物可用作油漆和涂料 | |
| C. | 氢化物的沸点:Z大于M | |
| D. | 工业上制备W单质的方法为电解熔融的W的氧化物 |
12.下列实验操作正确的是( )

| A. | 如图1,向容量瓶中转移溶液 | |
| B. | 图2,用标准浓度的NaOH溶液滴定未知浓度的盐酸 | |
| C. | 图3,实验室用浓硫酸和乙醇共热制乙烯 | |
| D. | 图4,验证H2在Cl2中燃烧的实验现象 |