题目内容
7.化学与生活息息相关,下列说法不正确的是( )| A. | 用食醋可除去热水壶内壁的水垢 | B. | 医用酒精的浓度通常为95% | ||
| C. | 烹鱼时加适量醋和酒可以增加香味 | D. | 碘盐中的碘不可以直接用淀粉检验 |
分析 A.水垢的成分为碳酸钙、氢氧化镁,可与酸发生复分解反应;
B.酒精浓度低不能杀死细菌,浓度太大在细胞壁形成一层膜,阻止酒精进入细胞内;
C.加适量醋和酒,生成具有香味的乙酸乙酯;
D.碘盐中的碘为碘酸钾,以化合物形式存在,淀粉遇碘单质变蓝.
解答 解:A.水垢的成分为碳酸钙、氢氧化镁,可与酸发生复分解反应,则食醋可除去热水壶内壁的水垢,故A正确;
B.酒精浓度低不能杀死细菌,浓度太大在细胞壁形成一层膜,阻止酒精进入细胞内,则医用酒精的浓度通常为体积分数为75%,故B错误;
C.加适量醋和酒,生成具有香味的乙酸乙酯,则可以增加香味,故C正确;
D.碘盐中的碘为碘酸钾,以化合物形式存在,淀粉遇碘单质变蓝,则碘盐中的碘不可以直接用淀粉检验,故D正确;
故选B.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
14.活动小组同学采用如图装置制备并测定所得固体中亚硝酸钠(NaNO2)的质量分数(装置可重复使用,部分夹持仪器已省略).

已知:
①2NO+Na2O2═2NaNO2;
②酸性条件下,NO、NO2都能与MnO4-反应生成NO3-和Mn2+;NaNO2能使
酸性高锰酸钾溶液褪色.
(1)实验装置的连接顺序为A C E D E B;
(2)C瓶内发生反应的离子方程式为Cu+2H++NO2=Cu2++NO↑+H2O.
(3)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,实验所得数据如表.
①下列选项导致结果偏高的是ad(填字母序号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶用蒸馏水洗净后未干燥
c.观察滴定终点时俯视读数
d.滴定结束,滴定管尖嘴端悬挂一滴液体
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为86.25%.
(4)设计实验,比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2电离程度的相对大小25℃时,将两种溶液等体积混合,若混合溶液的pH<7,则说明HNO2的电离程度大于NO2-的水解程度,若pH>7,则说明HNO2的电离程度小于NO2-的水解程度(简要说明实验步骤、现象和结论,仪器和药品自选).

已知:
①2NO+Na2O2═2NaNO2;
②酸性条件下,NO、NO2都能与MnO4-反应生成NO3-和Mn2+;NaNO2能使
酸性高锰酸钾溶液褪色.
(1)实验装置的连接顺序为A C E D E B;
(2)C瓶内发生反应的离子方程式为Cu+2H++NO2=Cu2++NO↑+H2O.
(3)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,实验所得数据如表.
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶用蒸馏水洗净后未干燥
c.观察滴定终点时俯视读数
d.滴定结束,滴定管尖嘴端悬挂一滴液体
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为86.25%.
(4)设计实验,比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2电离程度的相对大小25℃时,将两种溶液等体积混合,若混合溶液的pH<7,则说明HNO2的电离程度大于NO2-的水解程度,若pH>7,则说明HNO2的电离程度小于NO2-的水解程度(简要说明实验步骤、现象和结论,仪器和药品自选).
18.下列物质晶体类型和化学键类型完全相同的是( )
| A. | MgCl2 NaOH | B. | HCl SiO2 | C. | NaOH NH4Cl | D. | 红磷 金刚石 |
15.某有机物的结构简式为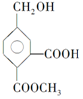 ,它在一定条件下可发生的反应为( )
,它在一定条件下可发生的反应为( )
①酯化反应 ②氧化反应 ③加聚反应 ④取代反应.
 ,它在一定条件下可发生的反应为( )
,它在一定条件下可发生的反应为( )①酯化反应 ②氧化反应 ③加聚反应 ④取代反应.
| A. | ①②④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
2.下列用途中所选用的物质正确的是( )
| A. | X射线透视肠胃的内服剂--碳酸钡 | |
| B. | 配制波尔多液原料--胆矾和石灰乳 | |
| C. | 生活用水的消毒剂--明矾 | |
| D. | 工业生产氯气的原料--浓盐酸和二氧化锰 |
12.设NA表示阿伏加得罗常数,下列叙述正确的是( )
| A. | 标准状况下,1mol氦气所含的原子数为2NA | |
| B. | 1.8g NH4+离子中所含的电子数为1.1NA | |
| C. | 常温常压下,44g二氧化碳分子中所形成的共用电子对数为4NA | |
| D. | NA个氮分子和NA个氢分子的体积相同 |
19.水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
| A. | 氨水的电离程度 | B. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | C. | c(H+)和c(OH-)的乘积 | D. | OH-的物质的量 |
16.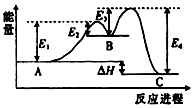 某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )
某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )
 某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )
某反应:A→C 由两步反应 A→B→C 完成,B 为中间产物,该反应能量曲线如图所示(E表示能量),下列有关叙述正确的是( )| A. | 两步反应均为吸热反应 | B. | 加入催化剂可以改变A→C的反应热 | ||
| C. | 三种化合物中C最稳定 | D. | 整个反应中△E=E4-E1-E2-E3 |
17.X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素.X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素.下列说法不正确的是( )
| Y | Z | M | |
| W |
| A. | 原子半径:W>Y>Z>M>X | |
| B. | N的一种氧化物可用作油漆和涂料 | |
| C. | 氢化物的沸点:Z大于M | |
| D. | 工业上制备W单质的方法为电解熔融的W的氧化物 |