题目内容
7.A是一种酯,分子式是C14H12O2,A可以由醇B跟羧酸C发生酯化反应得到.A不能使溴的CCl4溶液褪色.B连续氧化得到C.B的同分异构体都可以跟NaOH反应.写出A、B、C的结构简式:A.
 B.
B.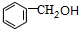 C.
C. .
.
分析 A的分子式是C14H12O2,不饱和度为$\frac{2×14+2-12}{2}$=9,酯A不能使溴的四氯化碳溶液褪色,所以其中有苯环,醇B氧化得羧酸C,说明了B和C分子中碳原子数相等,酯A中有14个碳原子,则B和C中各有7个碳原子,从而可判断B是苯甲醇,C是苯甲酸,A是苯甲酸苯甲酯.
解答 解:A的分子式是C14H12O2,不饱和度为:$\frac{2×14+2-12}{2}$=9,酯A不能使溴的四氯化碳溶液褪色,所以其分子中有苯环,
醇B氧化得羧酸C,说明了B和C分子中碳原子数相等,酯A中有14个碳原子,则B和C中各有7个碳原子,从而可判断B是苯甲醇,C是苯甲酸,A是苯甲酸苯甲酯,
故A的结构简式为: ,B结构简式为:
,B结构简式为: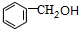 ,C的结构简式为:
,C的结构简式为: ,
,
故答案为: ;
;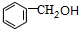 ;
; .
.
点评 本题考查有机物结构简式的确定,题目难度中等,涉及同分异构体及酯、醇、羧酸的性质等知识,明确常见有机物结构与性质为解答关键,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
相关题目
10.甲基叔丁基醚可制成针剂,用于治疗胆固醇型的胆结石病,在下列诸合成路线中,最佳合成路线是( )
| A. | 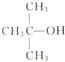 、CH3OH和浓硫酸共热 、CH3OH和浓硫酸共热 | B. | 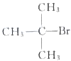 和CH3ONa共热 和CH3ONa共热 | ||
| C. | CH3Br和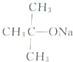 共热 共热 | D. |  和CH3OH在Al2O3存在下共热 和CH3OH在Al2O3存在下共热 |
2.MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果.某兴趣小组通过实验研究MnO2的性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是A.
A、把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B、把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C、把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成
D、把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比试验.该小组从上述对比实验中,可以得出的结论是酸性越强,MnO2氧化性越强.
写出在酸性条件下,MnO2氧化I-的离子方程式2I-+MnO2+4H+═I2+Mn2++2H2O.
(3)欲探究MnO2的催化效果,需要用30%的H2O2溶液(密度近似为1g/cm3)配制浓度3%的H2O2溶液(密度近似为1g/cm3)100mL.其配制方法是:用量筒量取10.0mL30%H2O2溶液放入烧杯(填仪器名称)中,再加入一定量的水,搅拌均匀.
(4)在实验时,某同学把1滴KI溶液误滴入到过量的5mL3%的H2O2溶液中,发现产生了大量气泡.该小组查阅到KI与H2O2可发生如下反应:2KI+H2O2=KOH+I2,认为有可能是反应产物I2起了催化H2O2分解的作用.请设计一个简单实验证明该假设是否正确.取5mL3%的H2O2溶液于试管中,滴入1滴碘水,观察是否有大量气泡产生,若有说明假设正确;反之假设不正确.
(5)实验室用二氧化锰和浓盐酸制取氯气,下列仪器可作为该反应的反应容器的是AD(填序号).

(6)二氧化锰可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,则其正极的电极反应式为2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是A.
A、把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B、把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C、把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成
D、把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比试验.该小组从上述对比实验中,可以得出的结论是酸性越强,MnO2氧化性越强.
写出在酸性条件下,MnO2氧化I-的离子方程式2I-+MnO2+4H+═I2+Mn2++2H2O.
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
(4)在实验时,某同学把1滴KI溶液误滴入到过量的5mL3%的H2O2溶液中,发现产生了大量气泡.该小组查阅到KI与H2O2可发生如下反应:2KI+H2O2=KOH+I2,认为有可能是反应产物I2起了催化H2O2分解的作用.请设计一个简单实验证明该假设是否正确.取5mL3%的H2O2溶液于试管中,滴入1滴碘水,观察是否有大量气泡产生,若有说明假设正确;反之假设不正确.
(5)实验室用二氧化锰和浓盐酸制取氯气,下列仪器可作为该反应的反应容器的是AD(填序号).

(6)二氧化锰可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,则其正极的电极反应式为2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O.
19.紫薯中含有被誉为“抗癌大王”的硒元素.已知硒原子的核电荷数为34,中子数为44,则硒原子的核外电子数为( )
| A. | 10 | B. | 34 | C. | 44 | D. | 78 |
16.关于0.1mol•L-1 H2SO4溶液的叙述错误的是( )
| A. | 1 L该溶液中含有H2SO4的质量为9.8 g | |
| B. | 将0.1mol H2SO4溶于1L水中可得该溶液 | |
| C. | 0.5 L该溶液中氢离子的物质的量浓度为0.2 mol•L-1 | |
| D. | 从1 L该溶液中取出100 mL,则取出溶液中H2SO4的物质的量浓度为0.1 mol•L-1 |
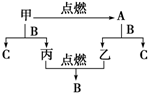 A、B、C是三种常见的化合物,A为淡黄色固体.它们之间的转化关系如图所示.完成下列空白:
A、B、C是三种常见的化合物,A为淡黄色固体.它们之间的转化关系如图所示.完成下列空白: