题目内容
18.化学反应原理在科研和生产中有广泛应用.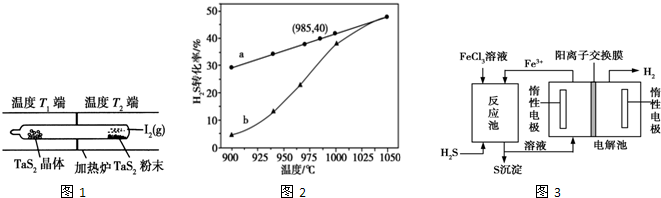
(1)SO2可用于制硫酸.已知25℃、101kPa时:2SO2(g)+O2(g)═2SO3(g)△H1=-197kJ/mol;
H2O(g)═H2O(l)△H2=-44kJ/mol;2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=-545kJ/mol.
则SO3(g)与H2O(l)反应的热化学方程式是SO3(g)+H2O(l)=H2SO4(l)△H=-130kJ/mol.
(2)利用“化学蒸气转移法”制备二硫化钽(TaS2)晶体,发生如下反应:TaS2(s)+2I2(g)═TaI4(g)+S2(g)△H>0(Ⅰ)
若反应(Ⅰ)的平衡常数K=1,向某恒容容器中加入1mol I2 (g)和足量TaS2(s),I2 (g)的平衡转化率为66.7%.
如图1所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2 (g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1<T2(填“>”“<”或“=”).上述反应体系中循环使用的物质是I2.
(3)利用H2S废气制取氢气的方法有多种.
①高温热分解法
已知:H2S(g)═H2(g)+$\frac{1}{2}$S2(g)△H4
在恒容密闭容器中,控制不同温度进行H2S分解实验.以H2S起始浓度均为c mol•L-1测定H2S的转化率,结果见图2.图2中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率.△H4>0(填>,=或<);说明随温度的升高,曲线b向曲线a逼近的原因:温度升高,反应速率加快,达到平衡所需的进间缩短.
②电化学法
该法制氢过程的示意图如图3.反应池中反应物的流向采用气、液逆流方式,其目的是增大反应物接触面积,使反应更充分;反应后的溶液进入电解池,电解总反应的离子方程式为2Fe2++2H+ $\frac{\underline{\;通电\;}}{\;}$2Fe3++H2↑.
分析 (1)2SO2(g)+O2(g)?2SO3(g)△H1=一197kJ/mol ①
2H2O (g)=2H2O(1)△H2=-88kJ/mol ②
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol③
利用盖斯定律:(③-①-②)×$\frac{1}{2}$ 得SO3(g)与H2O(l)反应的热化学方程式;
(2)设 I2的平衡转化率为x,则参加反应的I2为xmol,由方程式可知,平衡时生成TaI4和S2各0.5xmol,剩余I2为(1-x)mol,反应前后气体体积不变,可以用物质的量代替浓度计算平衡常数,根据K=$\frac{c(TaI{\;}_{4})×c(S{\;}_{2})}{c{\;}^{2}(I{\;}_{2})}$=1列方程计算;
该反应为吸热反应,温度T2端利于反应正向进行,应为高温,温度T1端利于反应向左进行,应为低温,反应中I2是可以循环使用的物质;
(3)①由图可知,随着温度升高,H2S的转化率也随之增大,所以升高温度平衡向正反应方向移动,正反应为吸热反应;
温度的升高,曲线b向曲线a逼近,反应速率加快,达到平衡时的时间缩短;
②反应池中反应物的流向采用气、液逆流方式,可增大反应物接触面积;电解池中亚铁离子失去电子,氢离子得到电子,以此来解答.
解答 解:(1)2SO2(g)+O2(g)2SO3(g)△H1=一197kJ/mol ①
2H2O (g)=2H2O(1)△H2=-88kJ/mol ②
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol③
利用盖斯定律:(③-①-②)×$\frac{1}{2}$ 得SO3(g)+H2O(l)=H2SO4(l)△H=-130kJ/mol,
故答案为:SO3(g)+H2O(l)=H2SO4(l)△H=-130kJ/mol;
(2)设 I2的平衡转化率为x,则参加反应的I2为xmol,由方程式可知,平衡时生成TaI4和S2各0.5xmol,剩余I2为(1-x)mol,反应前后气体体积不变,可以用物质的量代替浓度计算平衡常数,则K═$\frac{c(TaI{\;}_{4})×c(S{\;}_{2})}{c{\;}^{2}(I{\;}_{2})}$=$\frac{0.5x×0.5x}{(1-x){\;}^{2}}$=1,解得:x=66.7%;
该反应为吸热反应,一段时间后,在温度为T1的一端得到了纯净TaS2晶体,温度T2端利于反应正向进行,应为高温,温度T1端利于反应向左进行,应为低温,所以T1<T2,I2是可以循环使用的物质;
故答案为:66.7%;<;I2;
(3)①由图可知,随着温度升高,H2S的转化率也随之增大,所以升高温度平衡向正反应方向移动,正反应为吸热反应,所以△H4>0;
温度的升高,反应速率加快,达到平衡时的时间缩短,曲线b向曲线a逼近,
故答案为:>;温度升高,反应速率加快,达到平衡所需的进间缩短;
②反应池中反应物的流向采用气、液逆流方式,可增大反应物接触面积;电解池中亚铁离子失去电子,氢离子得到电子,电解总反应的离子方程式为2Fe2++2H+ $\frac{\underline{\;通电\;}}{\;}$2Fe3++H2↑,
故答案为:增大反应物接触面积,使反应更充分;2Fe2++2H+ $\frac{\underline{\;通电\;}}{\;}$2Fe3++H2↑.
点评 本题考查热化学方程式的书写、化学平衡有关计算与影响因素、化学平衡图象、电解原理等,是对学生综合能力的考查,难度中等.

| A. | 39g苯中含有C═C键数为1.5NA | |
| B. | 0.5molFeBr2与标准状况下33.6L氯气反应时转移电子数为3NA | |
| C. | 1L0.5mol•L-1的NaClO溶液中含有的ClO-离子数为0.5NA | |
| D. | 常温常压下,14g由C2H4和C3H6组成的混合气体中含有的原子总数为3NA |
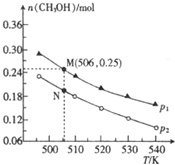
| A. | 甲中反应达到平衡时,Q1=Q | |
| B. | 达到平衡后,甲中C的体积分数比乙大 | |
| C. | 达到平衡后,再向乙中加入0.25molA、0.75molB、1.5molC,平衡向生成C的方向移动 | |
| D. | 乙中的热化学反应方程式为2C(g)?A(g)+3B(g)△H=+Q2kJ/mol |
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)•c(H2)=5c(CO)•c(H2O),试判断此时的温度 为700℃
(4)若830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,其化学平衡常数 K等于1.0(填“大于”“小于”或“等于”).
(5)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,扩大容器的体积,平衡不移动(填“向正反应方向”“向逆反应方向”或“不”).
(6)若1200℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时上述反应的平衡移动方向为逆反应方向(填“正反应方向”“逆反应方向”或“不移动”)
| A. | 常温下,反应C(s)+H2O(g)═CO(g)+H2(g)不能自发进行,则该反应的△H>0 | |
| B. | 一定温度下,反应MgCl2(l)═Mg(l)+Cl2(g)的△H>0,△S<0 | |
| C. | 放热的自发过程,一定是熵增加的过程 | |
| D. | 液态水可自发挥发成水蒸气的过程是熵减的过程 |
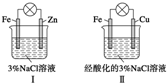
| A. | Ⅰ中不能形成原电池 | |
| B. | Ⅱ中负极反应是Fe-3e-═Fe3+ | |
| C. | Ⅱ中正极反应是O2+2H2O+4e-═4OH- | |
| D. | Ⅱ中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀 |
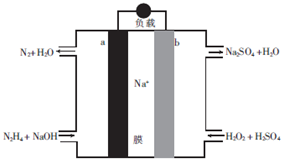
| A. | a极为电池的正极 | |
| B. | 电路中每转移6.02×1023个电子,则有1molNa+穿过膜向正极移动 | |
| C. | b极的电极反应式为H2O2+2e-=2OH- | |
| D. | 用该电池电解饱和食盐水,当阳极生成2.24L(标准状况)Cl2时,消耗肼0.1mol |
 以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.
以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法. B.
B.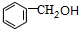 C.
C. .
.