题目内容
19.紫薯中含有被誉为“抗癌大王”的硒元素.已知硒原子的核电荷数为34,中子数为44,则硒原子的核外电子数为( )| A. | 10 | B. | 34 | C. | 44 | D. | 78 |
分析 依据在原子中,核电荷数=核外电子数分析解答.
解答 解:硒原子的核电荷数为34,根据在原子中,核电荷数=核外电子数,可知硒原子的核外电子数为34;
故选B.
点评 本题考查原子内结构,难度不大,利用在原子中,核电荷数=核外电子数的规律解决是解题的关键,属基础性知识考查题.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
9.可逆反应A(g)+3B(g)?2C(g)△H=-QkJ/mol(Q>0).有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2.下列叙述正确的是( )
| A. | 甲中反应达到平衡时,Q1=Q | |
| B. | 达到平衡后,甲中C的体积分数比乙大 | |
| C. | 达到平衡后,再向乙中加入0.25molA、0.75molB、1.5molC,平衡向生成C的方向移动 | |
| D. | 乙中的热化学反应方程式为2C(g)?A(g)+3B(g)△H=+Q2kJ/mol |
10.结合如图判断,下列叙述正确的是( )
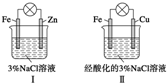

| A. | Ⅰ中不能形成原电池 | |
| B. | Ⅱ中负极反应是Fe-3e-═Fe3+ | |
| C. | Ⅱ中正极反应是O2+2H2O+4e-═4OH- | |
| D. | Ⅱ中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀 |
4.为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.供选择的化学试剂及实验方法
A.加热升华
B.加适量的食醋振荡
C.用pH试纸测定溶液pH
D.分别通入酸性高锰酸钾溶液.
| 实验目的 | 试剂及方法 |
| 除去细沙中混有的碘 | A |
| 证明某些雨水样品呈酸性 | C |
| 鉴别甲烷和乙烯 | D |
| 除去开水壶内壁的水垢 | B |
B.加适量的食醋振荡
C.用pH试纸测定溶液pH
D.分别通入酸性高锰酸钾溶液.
11.生活中的一些问题常涉及到化学知识,则下列叙述正确的是( )
| A. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 | |
| B. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| C. | 氯化铁溶液可用于制作印刷电路板是因为其具有较强氧化性,与铜发生置换反应 | |
| D. | 高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
8.一种直接肼燃料电池的结构如图所示,下列说法正确的是( )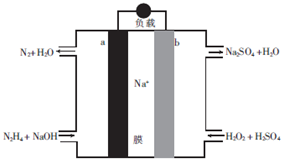

| A. | a极为电池的正极 | |
| B. | 电路中每转移6.02×1023个电子,则有1molNa+穿过膜向正极移动 | |
| C. | b极的电极反应式为H2O2+2e-=2OH- | |
| D. | 用该电池电解饱和食盐水,当阳极生成2.24L(标准状况)Cl2时,消耗肼0.1mol |
 B.
B. C.
C. .
. 发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.
发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.