��Ŀ����
1��ʵ������һ�ֹ�ҵ��������Ҫ�ɷ�ΪMgCO3��MgSO4������Fe��Al�������Ϊԭ���Ʊ�MgCO3?3H2O��ʵ�������ͼ1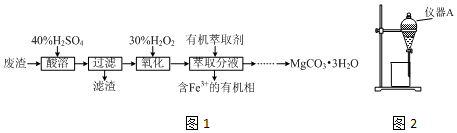
��1����������ȵ�Ŀ���Ǽӿ��������ʣ�����ʱ�õ��IJ���������©�� ������ �ձ�
��2������H2O2����ʱ������Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
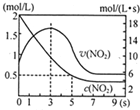
��3������ͼ2��ʾ��ʵ��װ�ý�����ȡ�ͷ�Һ���Գ�ȥ��Һ�е�Fe3+��
��ʵ��װ��ͼ2������A������Ϊ��Һ©����
��ΪʹFe3+�����ܶ�ش�ˮ��ת�����л��࣬��ȡ�IJ�������װ����Һ������A�м���һ�������л���ȡ������������á���Һ�����ظ���Σ�
���� ������Ҫ�ɷ�ΪMgCO3��MgSO4������Fe��Al�����������40%���������ܣ���������Һ�к�������þ�����������Լ�������������H2O2�����������ӣ�Ȼ������л���ȡ����ȡFe3+����Һ��ɳ�ȥ��Һ�е�Fe3+����Һ��ˮ��Һ�к���Mg2+��Al3+��Ȼ���ȥAl3+���پ���һϵ�в������õ�MgCO3•3H2O���Դ˽����⣮
��� �⣺��1�����ȣ��¶����ߣ�������Ӧ���ʣ����ӿ��������ʣ�����ʱ�õ��IJ��������У�©�� ������ �ձ���
�ʴ�Ϊ���ӿ��������ʣ�©�� ������ �ձ���
��2������H2O2��Һ����������ӷ���������ԭ��Ӧ����Ӧ�����ӷ���ʽΪ��2Fe2++2H++H2O2=2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++2H++H2O2=2Fe3++2H2O��
��3������װ��ͼ��֪����AΪ��Һ©����������ȡ����Һ��
�ʴ�Ϊ����Һ©����
����ȡʱ��Ϊʹ���ʾ����ܱ���ȡ��Ӧ������Գ�ֽӴ������룬
�ʴ�Ϊ�������
���� ���⿼�����ʵ��Ʊ�������������ᴿ����ȷ�����еķ����ͻ��������������Ļ�ѧ��Ӧ�ǽ��Ĺؼ���Ҫ��ѧ�����з����ͽ���������������Ŀ����������ѧ����ʵ����������Ŀ�Ѷ��еȣ�

| A�� | ����12.8gCuSO4�ܽ���100mLˮ�� | |
| B�� | ����25.0gCuSO4•5H2O��������100mLˮ�� | |
| C�� | ����16.0gCuSO4����ˮ��Ȼ��ϡ����100mL | |
| D�� | ����20.0gCuSO4•5H2O��������ˮ��Ȼ��ϡ����100mL |
��1����֪��C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ��mol-l
CO2��g��+H2��g��=CO��g��+H2O��g����H=+41.3kJ��mol-l
��̼��ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽΪC��s��+2H2O��g��=CO2��g��+2H2��g����H=+90.0kJ��mol-1���÷�Ӧ�ڸ��£�����¡��������¡����κ��¶ȡ����������������Է����У�
��2������̿��ԭ���ɴ������������NO�ȣ��������ķ�ӦΪC��s��+2NO��g��?N2��g��+CO2 ��g������ij�ܱ������м���һ�����Ļ���̿��NO����T1��ʱ����ͬʱ���õĸ������Ũ�������ʾ��
| ʱ�䣨min�� Ũ�ȣ�mol•L-1�� ���� | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������AD������ĸ����
A��ͨ��һ������NO B������һ�����Ļ���̿
C��������ʵĴ��� D���ݵ���С���������
��3���о���������ӦCO��g��+H2O��g��?H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯�����ʾ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |

| A�� | �÷�Ӧ���ڷֽⷴӦ | B�� | ͼ�е����ֻ����ﶼ���������� | ||
| C�� | �÷�Ӧ��Ԫ�صĻ��ϼ�û�б仯 | D�� | ��Ӧǰ��ԭ�ӵ�����ı� |
| A�� | Al3+ NH4+ Br- SO42- | B�� | Na+ Fe2+ Cl- NO3- | ||
| C�� | K+ Ba2+ Cl- NO3- | D�� | K+ Na+ SO42- SO32- |
 �����仯�����ڹ�ҵ���������������й㷺Ӧ�ã��ش��������⣺
�����仯�����ڹ�ҵ���������������й㷺Ӧ�ã��ش��������⣺��1�����������ȶ��������������������õ���ʽ��ʾ�������γɹ��̣�
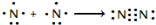 ��
����2��������N2H4����һ�ֻ�ԭ������֪��H2O��l���TH2O��g����H=+44kJ/mol���Խ���±����ݣ�д��N2H4 ��g��ȼ���ȵ��Ȼ�ѧ����ʽ��N2H4��g��+O2��g��=N2��g��+2H2O��l����H=-631.7kJ/mol��
| ��ѧ�� | N-H | N-N | N�TN | N��N | O�TO | O-H |
| ���ܣ�kJ/mol�� | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
��4�����Ĵ��������ڹ�ҵ�������ᣮ�÷�Ӧ����Ƴ����͵�أ���д�����Ի����£��õ�صĸ����缫��Ӧʽ��NH3-5e-+5OH-=NO+4H2O��
��5����ijŨ�ȵ�NO2�������һ���ݾ��������У�������Ӧ2NO2?N2O4�����ͼ����ͼ��
��0��3sʱv��NO2�������ԭ��������Ϊ������ϵ���÷�Ӧ������з��ȣ���ϵ�¶����ߣ�v��NO2������
��5sʱNO2ת����Ϊ75%��
 ��ͼ�������Լ�ƿ��ǩ�ϵ����ݣ�
��ͼ�������Լ�ƿ��ǩ�ϵ����ݣ�