题目内容
7.下列离子中半径最大的是( )| A. | O2? | B. | F- | C. | Mg2+ | D. | Al3+ |
分析 核外电子数相同,则核内质子数越多,对核外电子的吸引程度越大,半径越小.
解答 解:核外电子数相同,则核内质子数越多半径越小,所以离子半径为:F->Mg2+>Al3+;故选A.
点评 本题是一道有关元素周期律和元素周期表知识的题目,考查微粒半径大小比较的方法知识,难度一般.

练习册系列答案
相关题目
18.设NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 1 mol H2O所含有的原子数为3NA | |
| B. | 常温常压下,32g O2含有的氧原子数为2NA | |
| C. | 11.2L氯气所含的原子数为NA | |
| D. | 0.1mol•L -1NaCl溶液中c(Na+)为0.1 mol•L -1 |
12.下列说法正确的是( )
| A. | 钾(K)原子基态的原子结构示意图为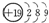 | |
| B. | Ca2+电子排布式为1s22s22p63s23p64s2 | |
| C. | 原子核内有10个中子的氧原子可表示为${\;}_{8}^{16}$O | |
| D. | H2O分子的电子式为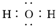 |
19.下列各组化合物中,化学键的类型完全相同的是( )
| A. | CaCl2和Na2S | B. | Na2O和Na2O2 | C. | CO2和NaCl | D. | HCl和NaOH |
16.不属于“氮的固定”的变化是( )
| A. | 豆科植物的根瘤菌固氮 | B. | .由氮气和氢气合成氨气 | ||
| C. | .雷雨天,空气中的氮气和氧气反应 | D. | .氨催化氧化制硝酸 |
17.下列化合物中,既含有离子键又含有共价键的是( )
| A. | H2O2 | B. | Na2O | C. | CO2 | D. | NaOH |
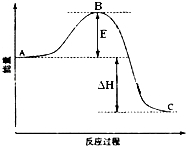 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题: 叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O=NaN3+NaOH+NH3,3NaNH2+NaNO3=NaN3+3NaOH+NH3↑.
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O=NaN3+NaOH+NH3,3NaNH2+NaNO3=NaN3+3NaOH+NH3↑. .
.