题目内容
18.设NA表示阿伏加德罗常数,下列叙述中不正确的是( )| A. | 1 mol H2O所含有的原子数为3NA | |
| B. | 常温常压下,32g O2含有的氧原子数为2NA | |
| C. | 11.2L氯气所含的原子数为NA | |
| D. | 0.1mol•L -1NaCl溶液中c(Na+)为0.1 mol•L -1 |
分析 A.1 mol H2O含有3mol原子;
B.O2只由氧原子构成来分析氧原子数;
C.常温常压不是标准状况,气体摩尔体积大于22.4L/mol;
D.1mol氯化钠电离出1mol氯离子.
解答 解:A.1 mol H2O含有3mol原子,原子数为3NA,故A正确;
B.O2只由氧原子构成,则氧原子的物质的量为$\frac{32g}{16g/mol}$=2mol,氧原子数为2mol×NA=2NA,故B正确;
C.常温常压下,气体摩尔体积大于22.4L/mol,11.2L氯气的物质的量小于0.5mol,含有的分子数小于0.5NA,故C错误;
D.钠离子浓度等于氯化钠浓度,为0.1 mol•L -1,故D正确.
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,气体摩尔体积的使用条件,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.下列反应中,不属于取代反应的是( )
| A. | 在催化剂存在条件下苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 在催化剂存在条件下,乙烯与氯化氢反应制氯乙烷 | |
| D. | 葡萄糖与银氨溶液反应 |
3.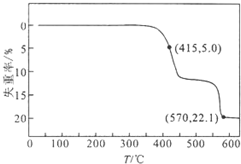 HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:
HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:
2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2C2O4+H2↑①
2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2↑+CO↑②
Na2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO↑③
下列说法正确的是( )
 HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:
HCOONa加热分解时,固体失重率与温度的关系如图所示,发生的反应有:2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2C2O4+H2↑①
2HCOONa$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2↑+CO↑②
Na2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO↑③
下列说法正确的是( )
| A. | T<415℃,只有反应①发生 | |
| B. | 反应①、②不可能同时发生 | |
| C. | 570℃<T<600℃时,残留固体的主要成分是Na2CO3 | |
| D. | 残留固体中的m(Na2C2O4)=m(Na2CO3)时,反应①、③的反应速率相等 |
7.下列离子中半径最大的是( )
| A. | O2? | B. | F- | C. | Mg2+ | D. | Al3+ |
8.下列叙述正确的是( )
| A. | 同主族元素自上而下,得电子能力增强 | |
| B. | 最外层电子数小于4的一定是金属元素 | |
| C. | 同周期元素中ⅠA族元素的原子半径最小 | |
| D. | 非金属:Cl>S>P |
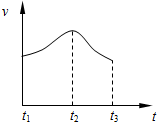 把除去氧化膜的镁条投入到盛有稀HCl的试管中,发现氢气发生的速率变化情况如图所示.
把除去氧化膜的镁条投入到盛有稀HCl的试管中,发现氢气发生的速率变化情况如图所示.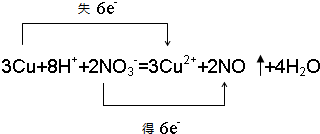 ,在这反应中该强酸展现酸性,氧化性.
,在这反应中该强酸展现酸性,氧化性.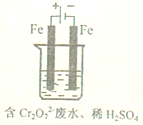 工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.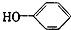 合成
合成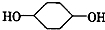 (部分试剂和反应条件已略去)
(部分试剂和反应条件已略去)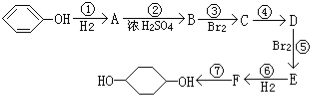
 ;F中含有官能团的名称为溴原子.
;F中含有官能团的名称为溴原子.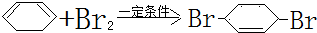 ,写出在同样反应条件下
,写出在同样反应条件下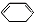 的化学方程式(有机物写结构简式,注明反应条件)
的化学方程式(有机物写结构简式,注明反应条件)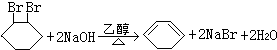 .
.