题目内容
4.下列涉及有机物的说法正确的是( )| A. | 2-己烯能使KMnO4(H+)溶液褪色 | |
| B. | 汽油、煤油、柴油和植物油都是碳氢化合物 | |
| C. | 乙烯、苯都可与溴水发生加成反应 | |
| D. | 乙烯和聚乙烯都能发生加聚反应 |
分析 A.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
B.植物油属于油脂;
C.苯性质较稳定,和溴水不反应;
D.聚乙烯中不含碳碳不饱和键.
解答 解:A.烯烃中含有碳碳双键,性质较活泼,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,可以用溴或酸性高锰酸钾溶液鉴别烷烃和烯烃,故A正确;
B.植物油中含有酯基,属于酯类化合物,为烃的含氧衍生物,故B错误;
C.苯性质较稳定,和溴水不反应,在溴化铁作催化剂条件下,和液溴发生取代反应生成溴苯,故C错误;
D.聚乙烯中不含碳碳不饱和键,性质较稳定,不能发生加聚反应,故D错误;
故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃、酯类物质、苯的性质,注意D中聚乙烯不含碳碳不饱和键,为易错点.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
14.下列说法中不正确的是( )
| A. | 共价化合物中不可能含有离子键 | |
| B. | 阴阳离子之间通过静电引力形成的化学键叫离子键 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 含有离子键的化合物一定是离子化合物 |
15.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1
已知的碳燃烧热△H1=a kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H2=c kJ•mol-1
S(s)+2K(s)═K2S(s)△H3=b kJ•mol-1
则x为( )
已知的碳燃烧热△H1=a kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H2=c kJ•mol-1
S(s)+2K(s)═K2S(s)△H3=b kJ•mol-1
则x为( )
| A. | 3a+b-c | B. | 3a-c+b | C. | a+b-c | D. | c-a-b |
12.香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法正确的是( )
| A. | 气态氢化物的沸点:W<T<R | |
| B. | 离子半径:T->R2- | |
| C. | 最高价氧化物对应的水化物碱性:Y>X | |
| D. | XR2、WR2两化合物含有的化学键的类型相同 |
9.下列排列顺序不正确的是( )
| A. | 热稳定性:HF>HCl>HBr | B. | 原子半径:Na>S>O | ||
| C. | 元素金属性:Na>Mg>Al | D. | 酸性:H3PO4>H2SO4>HClO4 |
16.某化学兴趣小组利用如图装置验证元素非金属性的变化规律.下列说法正确的是( )
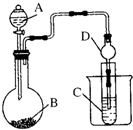

| A. | 仪器A的名称长颈漏斗,仪器 D的名称为球形干燥管 | |
| B. | 若利用上装置验证非金属性:Cl>S,装置A、B、C中所装药品应分别为稀盐酸、MnO2、Na2S溶液 | |
| C. | 若利用上装置证明非金属性:S>C>Si,装置A、B、C中所装药品应分别为稀硫酸、Na2CO3溶液、Na2SiO3溶液,观察到B中产生气泡,试管C中出现白色沉淀现象,则可以证明非金属性:S>C>Si | |
| D. | 装置A、B、C中所装药品应分别为稀盐酸、Na2CO3溶液、Na2SiO3溶液,观察到B中产生气泡,试管C中出现白色沉淀现象,则可以证明非金属性:Cl>C>Si |
13.将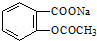 转变为
转变为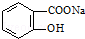 的方法为( )
的方法为( )
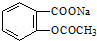 转变为
转变为 的方法为( )
的方法为( )| A. | 溶液加热,通入足量的HCl | |
| B. | 与足量的NaOH溶液共热后,再通入CO2 | |
| C. | 与稀H2SO4共热后,加入足量的Na2CO3 | |
| D. | 与稀H2SO4共热后,加入足量的NaOH |
14.要增大铁与盐酸反应的速率,所采取的下列措施中无效的是( )
| A. | 增大盐酸的浓度 | B. | 增大压强 | C. | 提高反应的温度 | D. | 用铁粉代替铁片 |