题目内容
4.在一定温度下的某容积不变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)?CO(g)+H2(g),下列叙述中不能认定上述可逆反应在一定条件下已达到化学平衡状态的是( )| A. | v正(CO)=v逆(H2O) | |
| B. | 2 mol H-O键断裂的同时有1 mol H-H键形成 | |
| C. | 生成n mol CO的同时生成n mol H2O(g) | |
| D. | 体系的压强不再发生变化 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、根据反应可知,自始至终v正(CO)=v正(H2O),若v正(CO)=v逆(H2O),则v正(H2O)=v逆(H2O),说明反应到达平衡,故A不符合;
B、断裂2mol H-O键同时生成l molH-H键,只能证明反应正向进行,不能说明反应到达平衡,故B符合;
C、根据反应可知,生成n mol CO的同时生成n mol H2O,说明正逆反应速率相同,能说明反应到达平衡,故C不符合;
D、因为是容积不变的密闭容器中,反应前后气体物质的量变化,当体系的压强不再发生变化,说明反应达平衡状态,故D不符合;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.已知乙烯醇不稳定,可自动转化成乙醛:CH2═CH-OH→CH3CHO.乙二醇在一定条件下发生脱水反应(有消去、有羟基和羟基之间反应形成“C-O-C”结构),所得产物的结构简式有人写出下列几种:
①CH2═CH2
②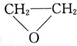
③CH3CHO
④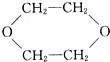
⑤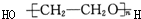
其中不可能的是( )
①CH2═CH2
②

③CH3CHO
④
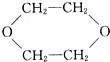
⑤
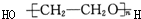
其中不可能的是( )
| A. | 只有① | B. | ②③ | C. | ③④ | D. | ④⑤ |
9.在一定温度下的定容容器中,发生反应:2A(g)+B(s)?C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①混合气体的压强不变
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④C(g)的物质的量浓度不变
⑤容器内A、C、D三种气体的浓度之比为2:1:1
⑥单位时间内生成n molD,同时生成2n mol A
⑦单位时间内生成n molC,同时消耗n molD.
①混合气体的压强不变
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④C(g)的物质的量浓度不变
⑤容器内A、C、D三种气体的浓度之比为2:1:1
⑥单位时间内生成n molD,同时生成2n mol A
⑦单位时间内生成n molC,同时消耗n molD.
| A. | ①②③ | B. | ②③④⑥⑦ | C. | ②③⑤⑥⑦ | D. | ①③⑤⑦ |
14.下面有关晶体的叙述中,错误的是( )
| A. | 白磷晶体中,分子之间通过共价键结合 | |
| B. | 金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | |
| C. | 在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-或(Na+) | |
| D. | 离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏 |