题目内容
6.空气吹出法工艺,是目前“海水提溴”的最主要方法之一.其工艺流程如下:
(1)步骤①获得Br2的离子反应方程式为:Cl2+2Br-═Br2+2Cl-;
(2)步骤③所发生反应的化学方程式为:Br2+SO2+2H2O═2HBr+H2SO4.在该反应中,氧化剂是Br2(填化学式);若反应中生成2molHBr,则转移电子数约为1.204×1024个.
(3)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是:Cl2>Br2>SO2
(4)步骤②通入热空气或水蒸气吹出Br2,利用了溴的C.
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(5)步骤⑤的蒸馏过程中,温度应控制在80~90℃.温度过高或过低都不利于生产,请解释原因:温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低.
(6)步骤⑥中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离.分离仪器的名称是分液漏斗.
(7)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低.
分析 海水提取氯化钠后得到苦卤,在卤水中通入氯气氧化溴在为溴单质,得到含溴单质的海水混合物Ⅰ,利用热空气和溴单质的挥发性吹出溴单质,得到含溴的空气,再用二氧化硫吸收得到吸收液,通入氯气氧化富集溴,得到溴水混合物Ⅱ,蒸馏得到溴蒸气冷凝分离得到液溴,
(1)步骤①获得Br2的离子反应是氯气氧化溴离子生成溴单质;
(2)步骤③所发生反应是溴单质和二氧化硫在水溶液中发生氧化还原反应生成硫酸和溴化氢,反应中元素化合价降低的物质做氧化剂,依据电子守恒和化学方程式定量关系计算电子转移总数;
(3)根据氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性进行判断;
(4)液溴易挥发分析;
(5)在溴水中,溴的沸点是58.5°C,水的是100°C,温度80℃-90℃时,水不沸腾而溴蒸气挥发;
(6)根据分液是分离两种不相溶的液体,用分液漏斗分离;
(7)海水中溴离子的浓度较少,在海水提取溴之前,必须进行海水浓缩以节约成本;
解答 解:(1)步骤①获得Br2的离子反应是氯气氧化溴离子生成溴单质,反应的离子方程式Cl2+2Br-═Br2+2Cl-,
故答案为:Cl2+2Br-═Br2+2Cl-;
(2)步骤③所发生反应是溴单质和二氧化硫在水溶液中发生氧化还原反应生成硫酸和溴化氢,反应的化学方程式为:Br2+SO2+2H2O═2HBr+H2SO4,反应中元素化合价降低的物质做氧化剂,负值溴单质中溴元素化合价降低,所以Br2为氧化剂,依据电子守恒和化学方程式定量关系计算电子转移总数,若反应中生成2molHBr,转移电子物质的量为2mol,则转移电子数约为2mol×6.02×1023/mol=1.204×1024,
故答案为:Br2+SO2+2H2O═2HBr+H2SO4; Br2; 1.204×1024;
(3)根据以上分析可知,氯气能够将溴离子氧化成溴单质,溴单质能够氧化二氧化硫,则说明氧化性强弱为:Cl2>Br2>SO2,
故答案为:Cl2>Br2>SO2;
(4)步骤②通入热空气或水蒸气吹出Br2,利用的是液溴易挥发,故选C,
故答案为:C;
(5)在溴水中,溴的沸点是58.5°C,水的是100°C,温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低,
故答案为:温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
(6)由于液溴与溴水不相溶,可用分液漏斗分离,
故答案为:分液漏斗;
(7)海水中溴离子的含量较少,在海水提取溴之前,必须进行海水浓缩,:“空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低;
故答案为:空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低;
点评 本题考查了海水资源的综合利用,题目难度中等,把握流程中发生的化学反应及混合物分离方法为解答的关键,注意掌握海水资源及其综合应用方法,试题培养了学生的分析能力及化学实验能力.

 智慧小复习系列答案
智慧小复习系列答案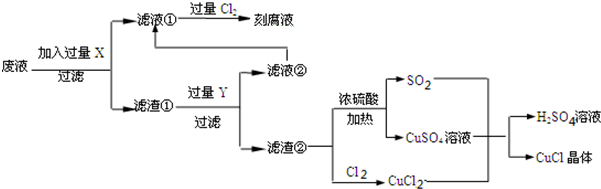
根据以上信息回答下列问题:
(1)该生产过程可以与氯碱工业、硫酸工业生产相结合,现代氯碱工业的装置名称是离子交换膜电解槽_此空删去.
(2)流程中的X是Fe,Y是HCl (均填化学式).
(3)产生CuCl的化学方程式为CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(4)为了提髙CuCl产品的质量,采用抽滤或者减压过滤法快速过滤,析出的CuCl晶体不用水洗涤而用无水乙醇洗涤,其目的是CuCl微溶于水、不溶于乙醇,用乙醇洗涤可减少产品CuCl的损失,生产过程中控制溶液的pH不能过大的原因是溶液pH大会促进CuCl的水解.
(5)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是防止CuCl的氧化和见光分解.
(6)氯化亚铜的定量分析:
①称取样品0.25g 置于预先放入10mL过量的FeCl3溶液250mL的锥形瓶中,不断摇动;
②待样品溶解后,加水50mL、邻菲罗啉指示剂2滴;
③立即用0.10mol•L-1硫酸铈Ce(SO4)2标准溶液滴至绿色出现为终点.同时做空白试验一次.已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+,如此再重复二次实验得到以下数据:
| 1 | 2 | 3 | |
| 空白试验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
④数据处理:计算得该工业CuCl的纯度为95%.(平行实验结果相差不能超过0.3%)
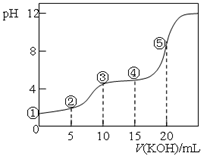 常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )
常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )| A. | 点①所示溶液中:c(H+)/c(OH-)=1012 | |
| B. | 点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) | |
| C. | 点③所示溶液中:c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.05mol•L-1 | |
| D. | 点⑤所示溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) |
| A. | 原子半径大小:Na>S>O | B. | 还原性强弱:F->Cl->Br->I- | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 气态氢化物稳定性:HBr>HCl>HF |
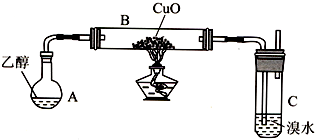
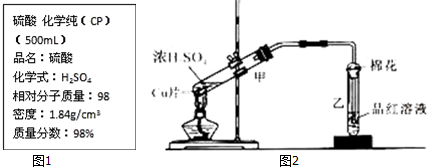
(1)实验开始时,对A进行水浴加热,其目的是产生平稳的乙醇气流.
(2)B中反应方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
(3)若装置C中开始发生倒吸,则采取的应急措施是C(填编号).
A.移去图中的酒精灯B.将C中橡皮塞上的短导气管拔出
C.将B尾端的乳胶管取下D.将A与B之间的乳胶管取下
(4)探究:充分反应后,观察到溴水完全褪色.学习小组通过测定反应前溴水中n(Br2)与反应后溶液中n(Br-)来确定乙醛使溴水褪色的原因.
①假设.请写出假设1的反应类型.
假设1:CH3CHO+Br2→CH2BrCHO+HBr;取代反应
假设2:CH3CHO+Br2→CH3CHBrOBr; 加成反应
假设3:CH3CHO+Br2+H2O→CH3COOH+2HBr. 氧化反应
②结论:若实验测得n(Br2)=0.005mol,n(Br-)=0.01mol,则证明假设3正确.
(5)欲检验乙醇中混有的少量乙醛,甲乙丙三同学设计实验如表:
| 试剂、用品 | 预期现象 | |
| 甲 | 酸性高锰酸钾溶液 | 溶液紫红色褪去 |
| 乙 | 溴水 | 溴水褪色 |
| 丙 | 铜丝 酒精灯 | 铜丝由黑色变成光亮的红色 |
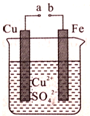
| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为Cu2++2eˉ=Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 | |
| D. | a和b用导线连接时,电流从铁片经导线流向铜片 |

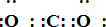 ;写出物质E的电子式:
;写出物质E的电子式: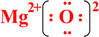 .
. NaCl
NaCl .
.