题目内容
10.用下图所示实验装置进行相应实验,能达到实验目的是( )| A. | 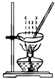 所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体 | |
| B. | 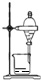 所示装置,分离CCl4萃取I2水后的有机层 | |
| C. | 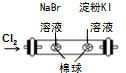 所示装置,证明氧化性:Cl2>Br2>I2 | |
| D. | 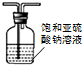 所示装置,除去SO2中混有的少量HCl气体 |
分析 A.氯化铵受热分解生成氯化氢和氨气;
B.互不相溶的液体采用分液方法分离;
C.同一氧化还原中,氧化剂的氧化性大于氧化产物的氧化性,氯气能氧化溴离子、碘离子;
D.亚硫酸钠和二氧化硫、HCl都反应.
解答 解:A.氯化铵受热分解生成氯化氢和氨气,所以不能采用蒸干氯化铵溶液制取氯化铵晶体,故A错误;
B.互不相溶的液体采用分液方法分离,四氯化碳和水不互溶,所以可以采用分液方法分离,故B正确;
C.同一氧化还原中,氧化剂的氧化性大于氧化产物的氧化性,氯气能氧化溴离子、碘离子,所以对溴的氧化性检验产生干扰,故C错误;
D.亚硫酸钠和二氧化硫、HCl都反应,应该用饱和的亚硫酸氢钠溶液除去二氧化硫气体中的HCl,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及物质准备、物质分离提纯、氧化性强弱比较等知识点,明确实验原理及物质性质是解本题关键,利用物质性质差异性选取合适的分离提纯方法,易错选项是C.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
20.在一定条件下的密闭容器中,一定能说明可逆反应:N2(g)+3H2(g)?2NH3(g)达到平衡状态的是( )
| A. | 混合气体的密度不再发生变化 | |
| B. | 反应速率之比υ(N2):υ(H2):υ(NH3)=1:3:2 | |
| C. | 每生成3molH2的同时消耗2molNH3 | |
| D. | 每断裂1molN≡N键的同时断裂6molN-H键 |
1.下列说法正确的是( )
| A. | 食盐水、稀豆浆、蔗糖水都能产生丁达尔效应 | |
| B. | 14C可用于文物的鉴定,14C与12C互为同素异形体 | |
| C. | 新能源汽车的推广与使用有助于减少光化学烟雾的产生 | |
| D. | 黑火药含有硫磺、硝酸钾和木炭,其中硝酸钾是电解质,硫磺和木炭是非电解质 |
5.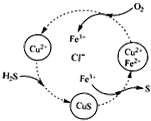 用含FeCl3、FeCl2、CuCl2的混合溶液和空气可吸收H2S并回收S,且能实现回收液的循环,其物质转化关系如图.下列有关说法错误的是( )
用含FeCl3、FeCl2、CuCl2的混合溶液和空气可吸收H2S并回收S,且能实现回收液的循环,其物质转化关系如图.下列有关说法错误的是( )
 用含FeCl3、FeCl2、CuCl2的混合溶液和空气可吸收H2S并回收S,且能实现回收液的循环,其物质转化关系如图.下列有关说法错误的是( )
用含FeCl3、FeCl2、CuCl2的混合溶液和空气可吸收H2S并回收S,且能实现回收液的循环,其物质转化关系如图.下列有关说法错误的是( )| A. | 氢、氯、铜三元素的化合价未发生改变 | |
| B. | 转化过程中包含三步化学反应 | |
| C. | 转化过程中还原剂为H2S和FeCl2 | |
| D. | 总反应可表示为:2H2S+O2→2S+2H2O |
2.下列有关化学与环境、生活的说法中,正确的是( )
| A. | 汽车尾气的排放是造成温室效应的主要原因 | |
| B. | 碘是人体必需的微量元素,但食用过量也会引起甲亢 | |
| C. | 纤维素在人体内可水解成葡萄糖,供人体组织的营养需要 | |
| D. | 明矾是常用的水处理剂,可用于城市自来水的杀菌消毒 |
19.四种短周期元素X、Y、Z、W的原子序数依次增大.X的最外层电子数是次外层电子数的2倍,Y、W同主族,Z是短周期中金属性最强的元素,X、W的质子数之和是Z的质子数的2倍.下列说法正确的是( )
| A. | 原子半径:X<Y<W<Z | |
| B. | 由 W与Y组成的分子都是非极性分子 | |
| C. | 由 Z与Y组成的化合物都能与水反应 | |
| D. | X与氢元素组成的化合物的沸点都低于Y与氢元素组成的化合物 |
20.给定条件下,下列选项中所示的物质间转化均能通过一步反应实现的是( )
| A. | Mg$→_{点燃}^{CO_{2}}$C$→_{△}^{H_{2}SO_{4}(浓)}$SO3 | |
| B. | 0.1mol•L-1HCl$→_{△}^{MnO_{2}}$Cl2$\stackrel{石灰水}{→}$Ca(ClO)2(aq) | |
| C. | NaCl饱和溶液$\stackrel{NH_{3}、CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | 淀粉溶液$→_{△}^{稀硫酸}$葡萄糖$→_{△}^{Cu(OH)_{2}悬浊液}$Cu2O |

 .
.