题目内容
常温时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、pH=0的溶液中:Na+、Fe2+、NO3-、ClO- | ||
| B、c(Fe3+)=0.1mol/L的溶液中:K+、Ba2+、SO42-、SCN- | ||
C、
| ||
| D、由水电离的c(H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=0的溶液呈酸性,NO3-、ClO-具有强氧化性;
B.与Fe3+反应的离子不能大量共存;
C.
=1012的溶液呈酸性;
D.由水电离的c(H+)=1×10-14 mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
B.与Fe3+反应的离子不能大量共存;
C.
| c(H+) |
| c(OH-) |
D.由水电离的c(H+)=1×10-14 mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
解答:
解:A.pH=0的溶液呈酸性,Fe2+、NO3-、ClO-发生氧化还原反应而不能大量共存,故A错误;
B.SCN-与Fe3+反应生成络合物,且Ba2+、SO42-反应生成沉淀,不能大量共存,故B错误;
C.
=1012的溶液呈酸性,酸性条件下离子之间不发生任何反应,可大量共存,故C正确;
D.由水电离的c(H+)=1×10-14 mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,无论呈酸性还是碱性,HCO3-都不能大量共存,故D错误.
故选C.
B.SCN-与Fe3+反应生成络合物,且Ba2+、SO42-反应生成沉淀,不能大量共存,故B错误;
C.
| c(H+) |
| c(OH-) |
D.由水电离的c(H+)=1×10-14 mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,无论呈酸性还是碱性,HCO3-都不能大量共存,故D错误.
故选C.
点评:本题考查离子的共存,为高考常见题型,侧重信息的抽取和离子反应的考查,注意氧化还原及互促水解为解答的难点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、油脂属于脂类 |
| B、蛋白质水解的最终产物是氨基酸 |
| C、纤维素不能发生水解反应 |
| D、淀粉完全水解的产物是葡萄糖 |
下列说法各选项中全部正确的是( )
①金属钠投入到FeCl2溶液中,最终有白色沉淀生成
②分液时,分液漏斗中的上层液体应由上口倒出
③加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3
④硅可用于制作光导纤维,因为硅是优良的半导体材料.
①金属钠投入到FeCl2溶液中,最终有白色沉淀生成
②分液时,分液漏斗中的上层液体应由上口倒出
③加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3
④硅可用于制作光导纤维,因为硅是优良的半导体材料.
| A、②③ | B、② | C、③④ | D、①②④ |
下列有关物质的分离说法正确的是( )
| A、可用加热法分离NH4Cl(s)和I2(s) |
| B、碘水中加CCl4振荡静置后,上层为紫色,下层几乎为无色 |
| C、工业上制无水酒精通常是将生石灰与95%酒精混合后蒸馏 |
| D、蒸馏、分馏和干馏都是利用组分沸点不同而分离的方法 |
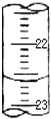 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: (其中M1、M2代表未知部分的结构),它在一定条件下可以发生如下转化:
(其中M1、M2代表未知部分的结构),它在一定条件下可以发生如下转化:
