题目内容
除去下列物质中的杂质(括号内为杂质),所选用的试剂和方法都正确的是( )
| 选项 | 物质 | 试剂 | 方法 |
| A | SiO2(Al2O3) | 氢氧化钠溶液 | 过滤 |
| B | AlCl3(MgCl2) | 氢氧化钠溶液 | 过滤 |
| C | CO2(SO2) | 饱和碳酸氢钠溶液 | 洗气 |
| D | 乙醇(水) | 汽油 | 萃取、分液 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用
专题:
分析:A.二者均与NaOH溶液反应;
B.二者均与NaOH溶液反应;
C.二氧化硫与碳酸氢钠反应,而二氧化碳不能;
D.乙醇中引入新杂质汽油.
B.二者均与NaOH溶液反应;
C.二氧化硫与碳酸氢钠反应,而二氧化碳不能;
D.乙醇中引入新杂质汽油.
解答:
解:A.二者均与NaOH溶液反应,不能除杂,应选稀盐酸、过滤,故A错误;
B.二者均与NaOH溶液反应,将原物质反应掉,不能除杂,故B错误;
C.二氧化硫与碳酸氢钠反应,而二氧化碳不能,则选择饱和碳酸氢钠、洗气可除杂,故C正确;
D.乙醇中引入新杂质汽油,不能除杂,应加CaO、蒸馏,故D错误;
故选C.
B.二者均与NaOH溶液反应,将原物质反应掉,不能除杂,故B错误;
C.二氧化硫与碳酸氢钠反应,而二氧化碳不能,则选择饱和碳酸氢钠、洗气可除杂,故C正确;
D.乙醇中引入新杂质汽油,不能除杂,应加CaO、蒸馏,故D错误;
故选C.
点评:本题考查混合物分离提纯,为高频考点,把握物质的性质及发生的反应、混合物分离方法选择为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
常温时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、pH=0的溶液中:Na+、Fe2+、NO3-、ClO- | ||
| B、c(Fe3+)=0.1mol/L的溶液中:K+、Ba2+、SO42-、SCN- | ||
C、
| ||
| D、由水电离的c(H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
下述实验方案能达到实验目的是.( )
| 编号 | A | B | C | D |
| 实验 方案 |  | 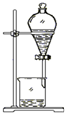 | 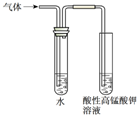 | 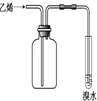 |
| 实验 目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
| A、A | B、B | C、C | D、D |
室温时,0.01mol?L-1HA溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,下列有关叙述正确的是( )
| A、原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B、当恰好完全中和时,溶液呈中性 |
| C、当滴入少量的NaOH,促进了HA的电离,溶液的pH升高 |
| D、当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
改变下列条件,一定能加快反应速率的是( )
| A、增加反应物的量 | B、增大压强 |
| C、加热 | D、加酶 |
以下物质间的每步转化中,不能通过一步反应实现的是( )
| A、FeCl2→Fe(OH)2→Fe(OH)3 |
| B、SO2→SO3→H2SO4 |
| C、Al→Al2O3→Al(OH)3 |
| D、NO→NO2→HNO3 |
将20 mL 0.3 mol/L AgNO3溶液与10 mL 0.4 mol/L CaCl2溶液混合,所得溶液中离子浓度关系正确的是( )
| A、c(NO3-)>c(Ca2+)>c(Cl-) |
| B、c(Ca2+)>c(NO3-)>c(Cl-) |
| C、c(Ca2+)>c(Cl-)>c(NO3-) |
| D、c(Cl-)>c(Ca2+)>c(NO3-) |
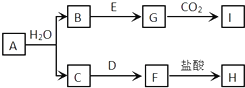
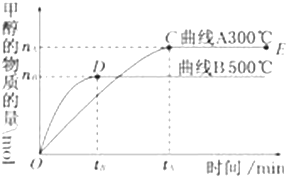 (1)一定条件下,在体积为4L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g).
(1)一定条件下,在体积为4L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g).