题目内容
19.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )
| A. | C60就是金刚石 | B. | C60属于有机化合物 | ||
| C. | C60的摩尔质量是720g/mol | D. | 1mol C60完全燃烧生成22.4L CO2 |
分析 C60是由碳元素形成的一种非金属单质,与石墨、金刚石等互为同素异形体,依据其化学式判断其摩尔质量、计算1mol完全燃烧产物的气体摩尔体积.
解答 解:A.C60是一种非金属单质,与金刚石互为同素异形体,故A错误;
B.此物质属于非金属单质,不是化合物,故B错误;
C.C60的相对分子质量为12×60=720,故摩尔质量是720g/mol,故C正确;
D.1mol C60完全燃烧生成标准状况下二氧化碳的物质的量为60mol,故体积为60×22.4L,故D错误,故选C.
点评 本题主要考查的是C60,应熟练掌握同素异形体的概念以及化合物和单质的概念,难度不大.

练习册系列答案
相关题目
9.向一定质量的Cu和Fe2O3的混合物中加入200mL3mol?L-1的HCl溶液,恰好使混合物完全溶解,向所得溶液中加入KSCN溶液中,无血红色出现.若过量的CO在高温下还原此混合物,得到固体的质量为( )
| A. | 17.6g | B. | 18.4g | ||
| C. | 24.0g | D. | 条件不足无法计算 |
10.下列各组溶液不能通过互滴实验进行鉴别的是( )
| A. | 碳酸钠 稀盐酸 | B. | 碳酸氢钠 稀盐酸 | ||
| C. | 氢氧化钠 氯化铝 | D. | 偏铝酸钠 稀硫酸 |
7.下列叙述一定正确的是( )
| A. | 两份质量相同的镁分别与足量氮气、二氧化碳反应,增重的质量相同 | |
| B. | 两份质量相同的硫分别与足量氢氧化钠和钠反应,两者转移的电子数相同 | |
| C. | 相同物质的量CO2、H2O分别与足量Na2O2反应,生成气体的体积相同 | |
| D. | 氢气分别通过灼热的CuO和Fe2O3粉末,当转移电子数相同时,固体减轻的质量相同 |
14.常温下,某同学设计实验验证H2SO3的酸性强于碳酸,下列实验方案能达到目的是( )
| 选项 | 实验方案 | 实验结果 |
| A | 将SO2气体依次通过NaHCO3溶液、溴水、品红溶液、澄清石灰水 | 品红无变化,澄清石灰水变浑浊 |
| B | 将过量二氧化硫气体通入碳酸氢钠溶液中,逸出的气体通入澄清石灰水 | 澄清石灰水变浑浊 |
| C | 取相同体积、相同物质的量浓度的NaHSO3与Na2CO3溶液,分别加入等体积、等浓度的少量盐酸 | 前者产生气体体积大于后者的 |
| D | 分别配置SO2和CO2的饱和溶液,立即测定两种饱和液的pH | 前者的pH小于后者的 |
| A. | A | B. | B | C. | C | D. | D |
4.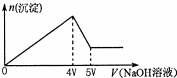 向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
 向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )| A. | 1:2 | B. | 1:1 | C. | 2:3 | D. | 3:2 |
11.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 酒精与水 | B. | 汽油与植物油 | C. | 溴与四氯化碳 | D. | 水与四氯化碳 |
8.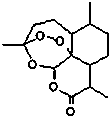 东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )
东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )
 东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )
东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )| A. | 分子式为C15H22O5 | |
| B. | 能够发生水解反应 | |
| C. | 用沸点只有35℃的乙醚作为溶剂来提取青蒿素的方法化学上叫萃取 | |
| D. | 青蒿素能够治疗疟疾可能与结构中存在过氧键或酯基等基团有关 |